题目内容
10.氨基磺酸(H2NSO3H)是一元固体强酸,溶于水和液氨,不溶于乙醇.在工业上用作酸性清洗剂、阻燃剂、磺化剂.用尿素[CO(NH2)2]和发烟硫酸(溶有SO3的硫酸)为原料合成氨基磺酸的稀的路线如下:
(1)“磺化”步骤中所发生的反应为:
①CO(NH2)2(s)+SO3(g)?H2NCONHSO3H(s)△H<0
②H2NCONHSO3H+H2SO4═2H2NSO3H+CO2↑
“磺化”过程应控制反应温度为75~80℃,若温度高于80℃,氨基磺酸的产率会降低,原因是温度高,SO3气体逸出加快,反应①平衡向逆反应方向移动,使反应①转化率降低;
(2)重结晶用10%~12%的硫酸作溶剂而不用水作溶剂的原因是氨基磺酸在硫酸溶液中的溶解度比在水中的溶解度小;
(3)测定产品中氨基磺酸纯度的方法如下:称取7.920g 产品配成l000mL待测液,量取25.00mL待测液于锥形瓶中,加入2mL 0.2mol•L-1稀盐酸,用淀粉碘化钾试剂作指示剂,逐滴加入0.08000mol•L-1NaNO2溶液,当溶液恰好变蓝时,消耗NaNO2溶液25.00mL,此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2.试求产品中氨基磺酸的质量分数.(请写出计算过程)
(4)以酚酞为指示剂,用NaOH进行酸碱中和滴定也能测定产品中氨基磺酸的纯度,测定结果通常比NaNO2法偏高,原因是氨基磺酸中混有硫酸杂质.
分析 (1)温度越高,三氧化硫的逸出速率越大,升高温度,平衡向吸热反应方向移动;
(2)根据溶质在不同溶剂中的溶解度大小分析;
(3)当溶液变蓝色时,说明H2NSO3H恰好完全反应,根据H2NSO3H和NaNO2之间的关系式计算H2NSO3H的物质的量,再根据质量分数公式进行计算;
(4)用氢氧化钠测定氨基磺酸的纯度,测定结果通常比NaNO2法偏高,说明还有其它物质和氢氧化钠反应.
解答 解:(1)温度越高,三氧化硫气体逸出速率加快,且CO(NH2)2(s)+SO3(g)?H2NCONHSO3H(s)是放热反应,温度高,SO3气体逸出加快,反应①平衡向逆反应方向移动,使反应①转化率降低,
故答案为:温度高,SO3气体逸出加快,反应①平衡向逆反应方向移动,使反应①转化率降低;
(2)反应H2NCONHSO3H+H2SO4?2H2NSO3H+CO2↑是可逆反应,硫酸浓度增大,平衡向正反应方向移动,所以能抑制氨基磺酸的溶解,
故答案为:氨基磺酸在硫酸溶液中的溶解度比在水中的溶解度小;
(3)①氨基磺酸与NaNO2溶液反应的化学方程式:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O,故答案为:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O;
②当溶液变蓝色时,说明H2NSO3H恰好完全反应,氨基磺酸和亚硝酸钠的反应方程式为:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O,
根据方程式知,n (H2NSO3H)=n(NaNO2)=25.00×l0-3×0.08000 mol•L-1=2.000×l0-3 mol,
ω(H2NSO3H)=$\frac{2.000×10{\;}^{-3}mol×97g/mol}{7.920g×\frac{25ml}{1000ml}}$×100%=98.0%,
故答案为:98.0%;
(4)用氢氧化钠测定氨基磺酸的纯度,测定结果通常比NaNO2法偏高,说明还有其它物质和氢氧化钠反应,能和氢氧化钠反应的物质是硫酸,故答案为:硫酸.
点评 本题考查测定物质的含量、化学平衡等知识点,会根据题给信息进行分析解答是解本题关键,难度较大.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| B. | C6H6十Br2$\stackrel{Fe}{→}$C6H5Br+HBr | |
| C. | CH2═CH2+Br2CH2Br-CH2Br | |
| D. | CH3COOH+CH3CH2OH$→_{加热}^{浓硫酸}$CH3COOCH2CH3+H2O |
| A. | 1 g Na2CO3 | B. | 0.1mol CaCO3 | C. | 56 g Fe | D. | 10 mLH2O |
| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| C. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| D. | 在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应 |
| A. | ①②④⑦ | B. | ①④ | C. | ③④⑥ | D. | ①③⑥ |
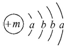 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.(1)m=20,该融雪剂的化学式为CaCl2.
(2)Z、W元素的名称为硫、碳.
(3)下列说法正确的是B
A.XY2和WZ2都为离子化合物 B.XY2分子中仅含离子键,WZ2中仅含共价键
C.H2Z比HY的稳定性强 D.X的阳离子比Y的阴离子半径大
(4)已知元素的电负性与元素的化合价一样,也是元素的一种基本性质.如表给出14种元素的电负性.
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | 碱性:KOH>NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 热稳定性:H2S>H2O>PH3>NH3 | D. | 原子半径:Na>S>O>F |
| A. | 在Na2CO3、NaHCO3两溶液中,离子种类不相同 | |
| B. | 在等体积、等物质的量浓度的Na2CO3、NaHCO3两溶液中,阳离子总数相等 | |
| C. | 在NaHCO3和Na2CO3混合溶液中一定有c(Na+)+c(H+)═c(HCO3-)+c(OH-)+2c(CO32-) | |
| D. | 在NaHCO3和Na2CO3混合溶液中一定有2c(Na+)=3[c(CO32-)+c(H2CO3)+c(HCO3-)] |