题目内容
16.下列关于金属性质的叙述中正确的是( )| A. | 钠与氧气反应时,产物只有一种 | |
| B. | 铝箔在空气中受热可以熔化且会发生剧烈燃烧 | |
| C. | 金属与非金属发生反应时,被氧化的一定是金属 | |
| D. | 铁丝不论在空气中还是纯氧中都不会燃烧 |
分析 A、钠和氧气反应产物不同时有反应条件决定;
B、铝在空气中不能燃烧;
C、金属原子结构可知金属单质一定失电子被氧化;
D、铁在纯氧气中燃烧生成四氧化三铁.
解答 解:A、钠和氧气反应产物不同时有反应条件决定,常温下钠和氧气反应生成氧化钠,钠点燃条件和氧气反应生成过氧化钠,故A错误;
B、铝箔在空气中受热可以熔化,但在空气中不能燃烧,故B错误;
C、金属原子结构可知金属单质一定失电子被氧化,金属与非金属发生反应时,被氧化的一定是金属,故C正确;
D、铁在纯氧气中燃烧生成四氧化三铁,空气中不能燃烧,故D错误;
故选C.
点评 本题考查了金属性质的分析,主要是反应条件、反应用量的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
4.X、Y、Z、W分别为短周期主族元素,原子序数依次增加,Y、Z为同周期相邻的元素,且四种元素分布在所有短周期中.四种元素原子最外层电子数之和为16,且W为金属元素.下列有关叙述正确的是( )
| A. | 常见单质的沸点:X<Y<W | B. | 简单氢化物的热稳定性:Y>Z | ||
| C. | 简单离子的半径:W>Y>Z | D. | 四种元素只能形成两种离子化合物 |
11.下列现象或事实不能用同一原理解释的是( )
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | SO2和Na2SO3溶液都能使氯水褪色 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | 硫化钠和亚硫酸钠固体长期暴露在空气中变质 |
1.化学与科学、技术、社会、环境密切相关,下列说法中正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 明矾净水的原理和“84”消毒液消毒的原理相同 | |
| C. | 为了防止中秋月饼等富脂食品氧化变质,延长保质期,可在包装袋中放入生石灰 | |
| D. | 光化学烟雾与大量排放碳氢化合物和氮氧化合物有关 |
8.某无色透明溶液,能跟金属铝反应产生H2,在该溶液中一定能大量存在的离子组( )
| A. | Mg2+ AlO2- | B. | Na+ SO42- | C. | Cu2+ SO42- | D. | Na+ CO32- |
6.下列各组中,可以用相同的方法除去混有的杂质的是( )
| A. | 淀粉溶液中混有少量NaCl与蔗糖中混有少量NaCl | |
| B. | Fe(OH)3胶体中混有少量盐酸与淀粉溶液中混有少量KI溶液 | |
| C. | Na2CO3中混有少量NaHCO3与NaHCO3中混有少量Na2CO3 | |
| D. | CO2中混有少量SO2与CO2中混有少量HCl气体 |
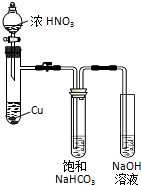 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: