题目内容
下列化学用语表示不正确的是( )
A、Na+的结构示意图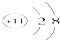 |
B、四氯化碳的电子式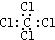 |
| C、二氧化碳的结构式为O=C=O |
| D、乙烯的实验式为 CH2 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.钠离子的核电荷数为11,核外电子总数为10,最外层为8个电子;
B.四氯化碳的电子式中,氯原子最外层达到8电子稳定结构,漏掉了3对未成键电子;
C.二氧化碳分子中存在两个碳氧双键,用短线代替所有共用电子对即为二氧化碳的结构式;
D.实验式为分子组成的最简比,根据乙烯的分子式确定其实验式.
B.四氯化碳的电子式中,氯原子最外层达到8电子稳定结构,漏掉了3对未成键电子;
C.二氧化碳分子中存在两个碳氧双键,用短线代替所有共用电子对即为二氧化碳的结构式;
D.实验式为分子组成的最简比,根据乙烯的分子式确定其实验式.
解答:
解:A.钠离子的核电荷数为11,最外层达到8电子稳定结构,钠离子的结构示意图为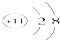 ,故A正确;
,故A正确;
B.四氯化碳为共价化合物,C、Cl原子都达到8电子稳定结构,四氯化碳正确的电子式为 ,故B错误;
,故B错误;
C.二氧化碳分子中存在两个碳氧双键,其电子式为: ,将共用电子对换成短线即为结构式,二氧化碳的结构式为:O=C=O,故C正确;
,将共用电子对换成短线即为结构式,二氧化碳的结构式为:O=C=O,故C正确;
D.乙烯的结构简式为:CH2=CH2,则乙烯的实验式为:CH2,故D正确;
故选B.
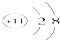 ,故A正确;
,故A正确;B.四氯化碳为共价化合物,C、Cl原子都达到8电子稳定结构,四氯化碳正确的电子式为
 ,故B错误;
,故B错误;C.二氧化碳分子中存在两个碳氧双键,其电子式为:
 ,将共用电子对换成短线即为结构式,二氧化碳的结构式为:O=C=O,故C正确;
,将共用电子对换成短线即为结构式,二氧化碳的结构式为:O=C=O,故C正确;D.乙烯的结构简式为:CH2=CH2,则乙烯的实验式为:CH2,故D正确;
故选B.
点评:本题考查了电子式、实验式、离子结构示意图、结构式的书写判断,题目难度中等,注意掌握常见化学用语的概念及书写方法,选项B为易错点,注意四氯化碳与甲烷电子式的区别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加快的是( )
| A、滴加少量硫酸铜溶液 |
| B、增多铁片的用量 |
| C、改用98%的浓硫酸 |
| D、加入少量的CH3COONa固体 |
X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大.Z和N可以形成ZN2型化合物.下列有关说法正确的是( )
| A、单质的氧化性:X<M |
| B、最高价氧化物对应水化物的碱性:Y>Z |
| C、气态氢化物的热稳定性:M>N |
| D、X与Y只能形成一种化合物 |
下列说法正确的是( )
| A、麦芽糖与蔗糖的水解产物均为葡萄糖,且均为二糖 |
| B、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| C、赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 |
| D、乙烯、氯乙烯、苯乙烯都是不饱和烃,均可用于合成有机高分子材料 |
下列变化过程属于放热反应的是( )
①浓硫酸的稀释
②碘的升华
③NaOH固体溶于水
④氢氧化钡晶体与氯化铵混合
⑤H2在Cl2中燃烧
⑥Al在高温条件下与Fe2O3 的反应 ⑦酸碱中和反应.
①浓硫酸的稀释
②碘的升华
③NaOH固体溶于水
④氢氧化钡晶体与氯化铵混合
⑤H2在Cl2中燃烧
⑥Al在高温条件下与Fe2O3 的反应 ⑦酸碱中和反应.
| A、①③⑤ | B、②④⑥ |
| C、⑤⑥⑦ | D、①③⑤⑥ |
在甲、乙两个体积不同的密闭容器中,分别充入质量相同的CO、CO2气体时,两容器的温度和压强均相同,则下列说法正确的是( )
| A、充入的CO分子数比CO2分子数少 |
| B、甲容器的体积比乙容器的体积小 |
| C、CO的摩尔体积比CO2的摩尔体积小 |
| D、甲中CO的密度比乙中CO2的密度小 |
甲苯  苯环上的一个氢原子被含3个碳原子的烷基所取代,可能得到的一元取代物有( )
苯环上的一个氢原子被含3个碳原子的烷基所取代,可能得到的一元取代物有( )
 苯环上的一个氢原子被含3个碳原子的烷基所取代,可能得到的一元取代物有( )
苯环上的一个氢原子被含3个碳原子的烷基所取代,可能得到的一元取代物有( )| A、3种 | B、4种 | C、5种 | D、6种 |
