题目内容
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 0.01mol•L-1氯水中,Cl2、Cl-和ClO-三粒子数目之和大于0.01NA | |
| B. | 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目2NA | |
| C. | 0.1molCu与足量的浓硫酸完全反应后,溶液中Cu2+数目为0.1NA | |
| D. | 2.0g D2O中含有的质子数、电子数均为NA |
分析 A.溶液体积未知;
B.气体状况未知,Vm不确定;
C.铜离子为弱碱阳离子,水溶液中部分水解;
D.1个D2O中含有10个质子,10个电子,摩尔质量是20g/mol.
解答 解:A.溶液体积未知,无法计算微粒数目,故A错误;
B.气体状况未知,Vm不确定,无法计算正极消耗气体的物质的量和电子转移数目,负极消耗气体分子数,故B错误;
C.铜离子为弱碱阳离子,水溶液中部分水解,所以1mol硫酸铜溶于水,溶液中铜离子数目小于0.1NA,故C错误;
D.1个D2O中含有10个质子,10个电子,则2.0g D2O物质的量为$\frac{2.0g}{20g/mol}$=0.1mol,含有的质子数、电子数均为NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意盐类水解规律,注意气体摩尔体积使用条件和对象,难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
1.所含分子数最少的物质是( )
| A. | 0.8molCO2 | B. | 标准状况下11.2L氨气 | ||
| C. | 3.6g水 | D. | 6.02×1023个水分子 |
2.将氢气、甲烷、乙醇等物质在氧气中嫩烧时的化学能直接转化为电能的装置叫燃料电池.此种电池能量利用率可高达80%,产物污染也少.下列有关燃料电池说法错误的是( )
| A. | 上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 | |
| B. | 氮氧燃料电池常用于肮天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇肮员使用 | |
| C. | 乙醇燃料电池的常用KOH溶液,该电池的负极反应为C2H5OH-12e-+3H2O═CO2↑+12H+ | |
| D. | 甲烷碱性燃料电池工作时OH-定向移动到负极 |
19.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 干冰只能用于人工降雨 | |
| B. | Al(OH)3可以治疗胃酸过多,因此可大量使用 | |
| C. | 为了增强去污效果,在洗衣粉中添加三聚磷酸钠(Na5P3O10) | |
| D. | 侯氏制碱法不涉及基本反应类型中的置换反应 |
6.下列关于物质或离子检验的叙述正确的是( )
| A. | 将气体通过湿润的淀粉KI试纸,试纸变蓝,证明原气体是Cl2 | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ | |
| D. | 将气体通过澄清石灰水,溶液变浑浊,证明原气体是CO2 |
16.如表是短周期的一部分,Y原子的核电荷数是X的2倍,下列关于这四种元素的说法正确的是( )
| X | ||
| M | Y | Z |
| A. | 氢化物沸点最高的是H2X | B. | M4的摩尔质量为124 | ||
| C. | X、Y、Z的简单离子半径最大的是Z | D. | X、Y两种元素,化合价都可以显-1价 |
3.欲使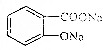 转变为
转变为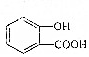 ,应用的试剂是( )
,应用的试剂是( )
 转变为
转变为 ,应用的试剂是( )
,应用的试剂是( )| A. | 盐酸 | B. | CO2 | C. | NaHCO3溶液 | D. | NaOH溶液 |
15.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2 L HF中含有分子的数目为0.5 NA | |
| B. | 0.1 mol Fe与少量氯气反应生成FeCl2,转移电子数为0.2 NA | |
| C. | 1.4 g由乙烯和环丙烷组成的混合物中含有原子的数目为 0.3 NA | |
| D. | 0.1 mol•L-1碳酸钠溶液中含有CO32-离子数目小于0.1 NA |
16.化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用.下列关于实验的叙述中正确的有( )
| A. | 不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抺布灭火 | |
| B. | 不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗 | |
| C. | 夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,并打开所有门窗通风 | |
| D. | 用氢气还原氧化铜时,先加热氧化铜,再通入氢气 | |
| E. | 可燃性气体点燃前一定要验纯 |