题目内容
如图所示的钢铁腐蚀中下列说法正确的是( )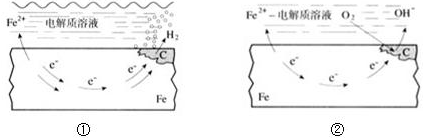

| A、碳表面发生氧化反应 |
| B、钢铁被腐蚀的最终产物为FeO |
| C、生活中钢铁制品的腐蚀以图①所示为主 |
| D、图②中,正极反应式为O2+4e-+2H2O═4OH- |
考点:金属的电化学腐蚀与防护
专题:
分析:根据图知,①为铁的析氢腐蚀,②为铁的吸氧腐蚀,酸性条件下钢铁发生消去反应,弱酸性或中性条件下钢铁发生吸氧腐蚀,在生活中钢铁主要以吸氧腐蚀为主,钢铁被腐蚀的最终产物是Fe2O3.xH2O,发生吸氧腐蚀时正极上氧气得电子发生还原反应.
解答:
解:根据图知,①为铁的析氢腐蚀,②为铁的吸氧腐蚀,
A.②为铁的吸氧腐蚀,该装置中Fe易失电子作负极、C作正极,正极上氧气得电子发生还原反应,故A错误;
B.Fe被氧化生成Fe 2+,Fe 2+和OH-反应生成Fe(OH)2,Fe(OH)2不稳定易被氧化生成Fe(OH)3,Fe(OH)3失水生成Fe2O3.xH2O,所以钢铁被腐蚀的最终产物是Fe2O3.xH2O而不是FeO,故B错误;
C.生活中钢铁主要以吸氧腐蚀为主,故C错误;
D.图②中铁发生吸氧腐蚀,正极反应式为O2+4e-+2H2O═4OH-,故D正确;
故选D.
A.②为铁的吸氧腐蚀,该装置中Fe易失电子作负极、C作正极,正极上氧气得电子发生还原反应,故A错误;
B.Fe被氧化生成Fe 2+,Fe 2+和OH-反应生成Fe(OH)2,Fe(OH)2不稳定易被氧化生成Fe(OH)3,Fe(OH)3失水生成Fe2O3.xH2O,所以钢铁被腐蚀的最终产物是Fe2O3.xH2O而不是FeO,故B错误;
C.生活中钢铁主要以吸氧腐蚀为主,故C错误;
D.图②中铁发生吸氧腐蚀,正极反应式为O2+4e-+2H2O═4OH-,故D正确;
故选D.
点评:本题考查金属的腐蚀与防护,明确钢铁发生析氢腐蚀和吸氧腐蚀的条件是解本题关键,知道各个电极上发生的反应,会正确书写电极反应式,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
常温下,在下列溶液中一定能大量共存的离子组是( )
| A、酸性溶液:Na+、Fe2+、AlO2-、SO42- |
| B、滴加石蕊试剂呈红色的溶液:Na+、Al3+、SO42-、Cl- |
| C、无色透明溶液:MnO4-、SO42-、K+、NO3- |
| D、强碱性的溶液:CO32-、NH4+、Cl-、Ca2+ |
某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程:则符合上述条件的酯的结构可能有( )
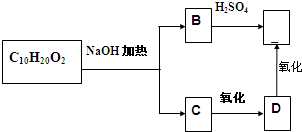

| A、2种 | B、8种 | C、6种 | D、4种 |
下图分别表示四种操作,其中有两处错误的是( )
A、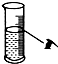 读数 |
B、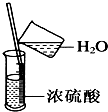 稀释 |
C、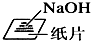 称量 |
D、 溶解 |
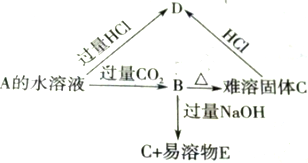 A、B、C、D、E 5种物质的转化关系如图所示.已知A为二元碱,微溶于水且溶解度随温度升高而降低
A、B、C、D、E 5种物质的转化关系如图所示.已知A为二元碱,微溶于水且溶解度随温度升高而降低