题目内容
3.浓度均为0.1mol/L的下列溶液中:①盐酸 ②硫酸 ③氢氧化钠 ④醋酸,pH值由小到大的顺序( )| A. | ①②④③ | B. | ③④②① | C. | ②①④③ | D. | ④②①③ |
分析 酸性溶液中氢离子浓度越大,溶液的pH越小;碱性溶液中氢氧根离子浓度越大,溶液的pH越大;盐酸、氢氧化钠为一元强电解质,硫酸为二元强酸,醋酸为弱酸,据此进行判断溶液的pH大小.
解答 解:浓度均为0.1mol/L的下列溶液中:①盐酸中氢离子浓度为0.1mol/L,溶液的pH=1;
②硫酸中氢离子浓度为:0.1mol/L×2=0.2mol/L,溶液的pH<1;
③氢氧化钠溶液中氢氧根氯离子浓度为0.1mol/L,溶液的pH=13;
④醋酸为弱酸,醋酸溶液中氢离子浓度小于0.1mol/L,溶液的pH>1;
根据分析可知,pH值由小到大的顺序为:②①④③,
故选C.
点评 本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握pH的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
13.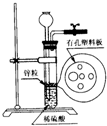 图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
①食盐水 ②BaCl2溶液 ③适量稀盐酸
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水 ⑦苯.
 图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( ) ①食盐水 ②BaCl2溶液 ③适量稀盐酸
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水 ⑦苯.
| A. | ①③⑤ | B. | ②⑥ | C. | ①②③⑤⑦ | D. | ①②④ |
14.实验室有下列试剂:①NaOH溶液 ②水玻璃 ③Na2S溶液④Na2CO3溶液⑤澄清的石灰水溶液 ⑥浓硫酸
其中必须用带橡胶塞的试剂瓶保存的是( )
其中必须用带橡胶塞的试剂瓶保存的是( )
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥ | D. | ①②③④⑤ |
8.综合如图判断,下列叙述不正确的是(Ⅱ中盐桥为KCl溶液)( )
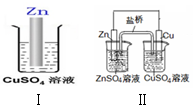

| A. | Ⅱ中盐桥中的Cl-移向ZnSO4溶液 | |
| B. | Ⅰ、Ⅱ的反应原理均是Zn+Cu2+=Zn2++Cu | |
| C. | Ⅰ、Ⅱ中均有电子转移,均是把化学能转化成电能利用 | |
| D. | 随着反应的进行,Ⅰ、Ⅱ中CuSO4溶液颜色均渐渐变浅 |
12.下列各组离子在指定条件下,一定能大量共存的是( )
| A. | pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- | |
| B. | 能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl- | |
| C. | 使酚酞变红的溶液:Ba2+、Na+、Cl-、NO3- | |
| D. | 能溶解Al(OH)3固体的溶液:K+、Na+、HCO3--、NO3-- |
13.实验测得常温下0.1mol/L某一元酸HA溶液的pH不等于l,0.1mol/L某一元碱BOH溶液里:$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12.将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
| A. | c(A-)>c(B+)>c(H+)>c(OH-) | B. | c(B+)>c(A-)>c(OH-)>c(H+) | ||
| C. | c(B+)+c (H+)>c(A-)+c(OH-) | D. | c(B+)>c(A-)>c(H+)>c(OH-) |
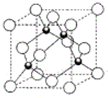 原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.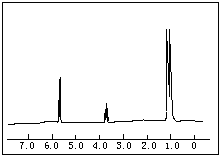 (1)已知1-丙醇和2-丙醇的结构简式如图:
(1)已知1-丙醇和2-丙醇的结构简式如图: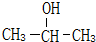
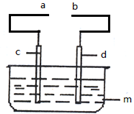 某小组为研究电化学原理,设计如图所示装置:
某小组为研究电化学原理,设计如图所示装置: