题目内容
苯乙烯是一种重要的有机化工原料,其结构简式如图,它一般不可能具有的性质是( )
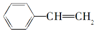
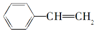
| A、易溶于水,不易溶于有机溶剂 |
| B、在空气中燃烧产生黑烟 |
| C、能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 |
| D、能发生加成反应,在一定条件下可与4倍物质的量的氢气加成 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有碳碳双键,可发生加成、加聚、氧化反应,含有苯环,可发生加成、取代反应,含有苯环常温下为液体,难溶于水,以此解答该题.
解答:
解:A.芳香烃都难溶于水,易溶于有机溶剂,故A错误;
B.含有苯环,碳的含量较高,在空气中燃烧产生黑烟,故B正确;
C.含有碳碳双键,可与溴水发生加成反应,可被酸性高锰酸钾氧化,故C正确;
D.含有碳碳双键,能发生加成反应,在一定条件下可与4倍物质的量的氢气加成,故D正确.
故选A.
B.含有苯环,碳的含量较高,在空气中燃烧产生黑烟,故B正确;
C.含有碳碳双键,可与溴水发生加成反应,可被酸性高锰酸钾氧化,故C正确;
D.含有碳碳双键,能发生加成反应,在一定条件下可与4倍物质的量的氢气加成,故D正确.
故选A.
点评:本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握有机物的官能团的性质,为解答该类题目的关键.

练习册系列答案
相关题目
“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用.下列化学反应,不符合绿色化学概念的是( )
| A、消除硫酸厂尾气排放的SO2:SO2+2NH3+H2O=(NH4)2SO3 |
| B、消除制硝酸工业尾气的氮氧化物污染:NO2+NO+NaOH=2NaNO2+H2O |
| C、制CuSO4:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O |
| D、制Cu(NO3)2:3Cu+8HNO3(稀)=3 Cu(NO3)2+2NO↑+4H2O |
X、Y是周期表中前20号中两种元素(非稀有气体元素),X原子的半径比Y的半径小,且具有相同的电子层数,下列有关叙述正确的是(选项中m、n均为正整数)( )
| A、若Y最高价为+5,则X最高价一定为+6或+7 |
| B、若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| C、若HnXOm为强酸,则X的氢化物溶液于水一定显酸性 |
| D、X的离子半径一定比Y离子半径小 |
往某溶液中通入过量氯气,再滴入Ba(NO3)2和HNO3溶液后,溶液中有白色沉淀,原溶液可能是( )
| A、AgNO3 |
| B、Na2SO3 |
| C、Na2CO3 |
| D、CaCl2 |
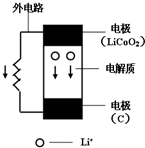 某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6| 充电 |
| 放电 |
| A、外电路上的“→”表示放电时的电流方向 |
| B、充电时阴极电极反应:LixC6-xe-═6C+xLi+ |
| C、放电时负极电极反应:LiCoO2-xe-═Li1-xCoO2+xLi+ |
| D、外电路有0.1mol e-通过,发生迁移的Li+的质量为0.7g |
下列离子方程式中正确的是( )
| A、石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
| B、硫酸铝溶液中滴加过量氨水:Al3++4OH-=AlO2-+2H2O |
| C、FeBr2溶液与足量Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
| D、向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
铝、氧化亚铁、氧化铁三种物质的均匀混合物分为两等份,一份直接与足量的烧碱反应,放出标况下16.8L气体.另一份在高温条件下恰好发生铝热反应,然后向反应后的混合物中加足量的稀盐酸,产生标况下的气体体积可能是( )
| A、22.4 | B、16.8 |
| C、15.2 | D、21.6 |
阿伏加德罗常数为NA,下列说法中正确的是( )
| A、1.0L 1.0 mol?L-1NaNO3溶液中含有的氧原子数为3NA |
| B、在标准状况下,22.4LCO2和O2混合气体中含有的氧原子数为NA |
C、 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA |
| D、0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA |