题目内容
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 30mL盐酸 | 30mL盐酸 | 30mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、向50 mL盐酸中加入混合物27.6 g时,盐酸过量 |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、15.7 g混合物与盐酸恰好能完全反应 |
| D、盐酸的物质的量浓度为5.0 mol/L |
考点:有关混合物反应的计算,钠的重要化合物
专题:计算题
分析:盐酸同量,由于第二组实验所得气体多于第一组实验,说明加入混合物9.2 g时盐酸过量,第二组与第三组所得气体相等,说明第二组盐酸完全反应,生成3.36L二氧化碳需要混合物的质量为
×9.2g=13.8g<15.7g,故第二组混合物有剩余、盐酸完全反应;
A.第二组实验中盐不足,混合物有剩余,第二组实验中发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为0.15mol,由方程式可知n(HCl)=n(CO2),据此计算盐酸的物质的量浓度,进而计算50mL溶液中HCl的物质的量,根据第一组生成二氧化碳的体积计算27.6g混合物反应消耗HCl的物质的量,据此判断;
B.设9.2 g混合物中NaHCO3、KHCO3的物质的量分别为xmol和ymol,根据碳元素守恒可知n(CO2)=n(NaHCO3)+n(KHCO3),再利用混合物质量列方程计算x、y的值,进而计算混合物中NaHCO3的质量分数;
C.根据A的分析判断;
D.根据A中的计算判断.
| 3.36L |
| 2.24L |
A.第二组实验中盐不足,混合物有剩余,第二组实验中发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为0.15mol,由方程式可知n(HCl)=n(CO2),据此计算盐酸的物质的量浓度,进而计算50mL溶液中HCl的物质的量,根据第一组生成二氧化碳的体积计算27.6g混合物反应消耗HCl的物质的量,据此判断;
B.设9.2 g混合物中NaHCO3、KHCO3的物质的量分别为xmol和ymol,根据碳元素守恒可知n(CO2)=n(NaHCO3)+n(KHCO3),再利用混合物质量列方程计算x、y的值,进而计算混合物中NaHCO3的质量分数;
C.根据A的分析判断;
D.根据A中的计算判断.
解答:
解:A.盐酸同量,由于第二组实验所得气体多于第一组实验,说明加入混合物9.2 g时盐酸过量,第二组与第三组所得气体相等,说明第二组盐酸完全反应,生成3.36L二氧化碳需要混合物的质量为
×9.2g=13.8g<15.7g,故第二组混合物有剩余、盐酸完全反应,
第二组实验中盐不足,混合物有剩余,第二组实验中发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为
=0.15mol,由方程式可知n(HCl)=n(CO2)=0.15mol,盐酸的物质的量浓度为
=5mol/L,
则50mL盐酸中HCl为0.05L×5mol/L=0.25mol,第一组中混合物完全反应,由方程式可知,消耗n(HCl)=n(CO2)=
=0.1mol,故27.6g混合物完全反应消耗HCl为0.1mol×
=0.3mol>0.25mol,故向50 mL盐酸中加入混合物27.6 g时,盐酸不足,故A错误;
B.第一组实验中混合物完全反应,盐酸过量,发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为
=0.1mol,设9.2 g混合物中NaHCO3、KHCO3的物质的量分别为xmol和ymol,根据碳元素守恒可知:x+y=0.1mol,混合物质量为9.2g,所以84x+100y=9.2g,联立方程解得x=0.05 mol,y=0.05 mol,能计算NaHCO3的质量分数,故B错误;
C.由A分析可知,15.7 g混合物与盐酸反应时,盐酸不足,固体混合物由剩余,故C错误;
D.由A分析可知,盐酸的物质的量浓度为5mol/L,故D正确;
故选D.
| 3.36L |
| 2.24L |
第二组实验中盐不足,混合物有剩余,第二组实验中发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为
| 3.36L |
| 22.4L/mol |
| 0.15mol |
| 0.03L |
则50mL盐酸中HCl为0.05L×5mol/L=0.25mol,第一组中混合物完全反应,由方程式可知,消耗n(HCl)=n(CO2)=
| 2.24L |
| 22.4L/mol |
| 27.6g |
| 9.2g |
B.第一组实验中混合物完全反应,盐酸过量,发生反应H++HCO3-═CO2↑+H2O,生成二氧化碳的物质的量为
| 2.24L |
| 22.4L/mol |
C.由A分析可知,15.7 g混合物与盐酸反应时,盐酸不足,固体混合物由剩余,故C错误;
D.由A分析可知,盐酸的物质的量浓度为5mol/L,故D正确;
故选D.
点评:本题考查混合物的计算,题目难度中等,根据二氧化碳的体积变化判断盐酸是否完全反应是关键,侧重考查学生对合物知识掌握及数据分析处理能力,较好的考查学生的思维能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图实验装置或操作与微粒的大小无直接关系的是( )
A、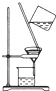 过滤 |
B、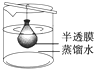 渗析 |
C、 萃取 |
D、 丁达尔效应 |
根据如表的数据,判断下列说法正确的是( )
| 离子化合物 | 离子电荷数 | 晶格能 kJ?mol-1 | 熔点 °C | 莫氏硬度 |
| NaF | 1 | 923 | 993 | 3.2 |
| NaCl | 1 | 786 | 801 | 2.5 |
| MgO | 2 | 3791 | 2852 | 6.5 |
| CaO | 2 | 3401 | 2614 | 4.5 |
| A、晶格能的大小与正负离子电荷数和距离成正比 |
| B、NaF晶体比NaCl晶体稳定 |
| C、表中物质CaO的晶体最稳定 |
| D、晶格能就是正负离子间的静电引力,晶格能越大,晶体的熔点越高,硬度越大 |
近年来我国大部分地区常被雾霾笼罩,PM2.5数据持续“爆表”,严重影响人们的身体健康.PM2.5是指大气中直径小于或等于2.5 μm(微米)的细小颗粒物,也称为可入肺颗粒物,它是大气的一种污染物,主要来自化石燃料的燃烧等.下列有关说法不正确的是( )
| A、“雾霾”不属于自然现象 |
| B、PM2.5的产生与人类活动有关 |
| C、PM2.5分散在空气中形成的混合物具有丁达尔效应 |
| D、开发利用新能源,减少化石燃料的使用是缓解雾霾天气发生的重要措施 |
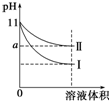 某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示.据图判断错误的是( )
某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示.据图判断错误的是( )| A、a的数值一定大于9 |
| B、Ⅱ为氨水稀释时溶液的pH变化曲线 |
| C、稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
| D、完全中和相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水) |
将一块严重锈蚀而部分变成铜绿[Cu2(OH)2CO3]的铜块研磨成粉末,在空气中充分灼烧成CuO,固体质量的变化情况不可能是( )
| A、增重10% | B、增重30% |
| C、不变 | D、减轻20% |