题目内容
3.下列叙述正确的是( )| A. | 标准状况下,22.4LCl2完全反应转移电子数一定为2×6.02×1023 | |
| B. | 因SO2具有漂白性,故可使品红溶液、酸性KMnO4溶液褪色 | |
| C. | 常温下,$\frac{c(OH-)}{c(H+)}$=10-10的溶液中:Na+、Al3+、SO42-、NO3-可大量共存 | |
| D. | 将20.0gNaOH固体置入500mL容量瓶,然后加水至刻度线即得1.00mol/L的NaOH溶液 |
分析 A、假设氯气与氢氧化钠溶液的反应,1mol氯气完全反应转移1mol电子,据此分析;
B、二氧化硫和高锰酸钾之间发生的是氧化还原反应;
C、常温下,氢氧根离子和氢离子浓度之比等于10-10的溶液是酸性溶液,据此回答;
D、容量瓶不能作为溶解固体的仪器使用.
解答 解:A、假设氯气与氢氧化钠溶液的反应,标准状况下,22.4LCl2完全反应转移电子数为6.02×1023,故A错误;
B、二氧化硫和高锰酸钾之间发生的是氧化还原反应,二氧化硫使酸性KMnO4溶液褪色,表现的是二氧化硫的还原性,故B错误;
C、常温下,氢氧根离子和氢离子浓度之比等于10-10的溶液是酸性溶液,Na+、Al3+、SO42-、NO3-可大量共存,故C正确;
D、容量瓶不能作为溶解固体的仪器使用,应该在烧杯中溶解再移入容量瓶中,故D错误.
故选C.
点评 本题综合考查学生氧化还原反应中电子转移、二氧化硫的漂白性、离子共存以及容量瓶的使用原理等知识,属于综合知识的考查,难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
14.有温度和容积均相同的两容器Ⅰ、Ⅱ,向Ⅰ中加入1mol NO2,Ⅱ中加入2mol NO2,都将发生反应2NO2(g)?N2O4(g),反应达到平衡时,测得Ⅰ中NO2的转化率为a%,Ⅱ中NO2的转化率为b%,则a、b的关系为( )
| A. | a<b | B. | a>b | C. | a=b | D. | 无法确定 |
11.下列关于各实验装置的叙述中,正确的是( )
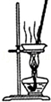 | 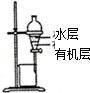 |
| A.装置可用于蒸干氯化铝溶液制AlCl3 | B.装置可用于分离CCl4萃取碘水后已分层的有机层和水层 |
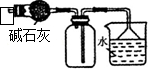 | 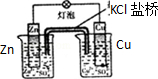 |
| C.装置可用于收集NH3或HCl气体,并防止倒吸 | D.装置盐桥中的K+自右向左移动 |
| A. | A | B. | B | C. | C | D. | D |
18.有以下七种饱和溶液(1)Ba(NO3)2 (2)Ca(OH)2 (3)Na2SiO3 (4)CaCl2 (5)Na2CO3
(6)NaAlO2 (7)NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是( )
(6)NaAlO2 (7)NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是( )
| A. | ②③④⑥ | B. | ①③⑥ | C. | ③⑤⑥⑦ | D. | ②③⑥ |
15.在一密闭容器中,充入一定量的反应物A,反应 aA(g)?bB(g)达平衡后,保持温度不变,将容器体积缩到一半,当达到新的平衡时,B的浓度是原来的1.6倍,则( )
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | 物质B的质量增重了 | D. | a>b |
12.用惰性电极进行电解,下列说法正确的是( )
| A. | 电解稀硫酸溶液,实质上是电解水,故溶液中c(H+)不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液中c(OH-)减小 | |
| C. | 电解硫酸钠溶液,在阴极上和阳极上析出的产物的物质的量之比为1:2 | |
| D. | 电解硝酸银溶液,在阴极上和阳极上析出的产物的物质的量之比可能不为4:1 |
 HCO3-+H+
HCO3-+H+