题目内容
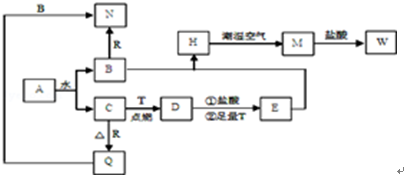
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出 现血红色.
(1)写出下列物质的化学式:D: E: N:
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象: 此过程发生的化学反应方程式
(3)检验E中阳离子的方法
(4)写出下列转化的离子方程式或化学方程式.
①A与水反应的离子方程式
②Q+B→N的离子方程式 .

(1)写出下列物质的化学式:D:
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:
(3)检验E中阳离子的方法
(4)写出下列转化的离子方程式或化学方程式.
①A与水反应的离子方程式
②Q+B→N的离子方程式
考点:无机物的推断
专题:
分析:依据转化关系和反应条件,A为淡黄色固体判断为Na2O2,D是具有磁性的黑色晶体判断为Fe3O4,C是无色无味的气体是过氧化钠与水反应生成的氧气,B为NaOH,W溶液中加入KSCN出现血红色,说明W含有三价铁离子;T、R为两种常见的用途很广的金属单质,T在C中燃烧生成D为四氧化三铁,溶于盐酸生成溶液中含有亚铁离子和三价铁离子,加入过量铁反应生成亚铁离子,证明T为Fe;E为FeCl2,H为Fe(OH)2,M为Fe(OH)3,W为FeCl3;金属R与B氢氧化钠反应说明R金属为Al,N为NaAlO2,Q为Al2O3,依据判断出各物质回答问题.
解答:
解:A为淡黄色固体判断为Na2O2,D是具有磁性的黑色晶体判断为Fe3O4,C是无色无味的气体是过氧化钠与水反应生成的氧气,B为NaOH,W溶液中加入KSCN出现血红色,说明W含有三价铁离子;T、R为两种常见的用途很广的金属单质,T在C中燃烧生成D为四氧化三铁,溶于盐酸生成溶液中含有亚铁离子和三价铁离子,加入过量铁反应生成亚铁离子,证明T为Fe;E为FeCl2,H为Fe(OH)2,M为Fe(OH)3,W为FeCl3;金属R与B氢氧化钠反应说明R金属为Al,N为NaAlO2,Q为Al2O3,
(1)依据判断得到DEN的化学式分别为:D为Fe3O4 ,E为FeCl2,N为NaAlO2,故答案为:Fe3O4 ;FeCl2;NaAlO2;
(2)B与E混和得到H为白色氢氧化亚铁沉淀,在潮湿空气中变成红褐色氢氧化铁沉淀的过程中,可能观察到的现象是:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色,反应方程式为4 Fe(OH)2+O2+2H2O═4 Fe(OH)3,故答案为:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色;4 Fe(OH)2+O2+2H2O═4 Fe(OH)3;
(3)若向溶液中加入铁氰化钾,有蓝色沉淀生成,说明含有二价铁离子,故答案为:向溶液中加入铁氰化钾,有蓝色沉淀生成;
(4)①Na2O2与水反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,
②Al2O3与NaOH反应生成NaAlO2的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;Al2O3+2OH-=2AlO2-+H2O.
(1)依据判断得到DEN的化学式分别为:D为Fe3O4 ,E为FeCl2,N为NaAlO2,故答案为:Fe3O4 ;FeCl2;NaAlO2;
(2)B与E混和得到H为白色氢氧化亚铁沉淀,在潮湿空气中变成红褐色氢氧化铁沉淀的过程中,可能观察到的现象是:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色,反应方程式为4 Fe(OH)2+O2+2H2O═4 Fe(OH)3,故答案为:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色;4 Fe(OH)2+O2+2H2O═4 Fe(OH)3;
(3)若向溶液中加入铁氰化钾,有蓝色沉淀生成,说明含有二价铁离子,故答案为:向溶液中加入铁氰化钾,有蓝色沉淀生成;
(4)①Na2O2与水反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,
②Al2O3与NaOH反应生成NaAlO2的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;Al2O3+2OH-=2AlO2-+H2O.
点评:本题考查了物质转化关系的应用判断,物质性质的应用,主要考查铝及其化合物、铁及其化合物性质的应用,化学方程式、离子方程式书写方法,离子检验方法,物质的特征反应、现象、性质是解题关键.

练习册系列答案
相关题目
化学与生活、生产和环境等社会实际密切相关.下列说法正确的是( )
| A、处理废水时加入明矾作为消毒剂可以除去水中的杂质 |
| B、利用铜、锶、钡等金属化合物的焰色反应制造节日烟花 |
| C、高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
| D、PM2.5含有的铅、镉、铬、钒、砷等元素均为对人体有害的金属元素 |
设NA为阿伏加德常数的值,下列说法正确的是( )
| A、32gSO2含有2NA个S=O键 |
| B、0.3 mol NO2与足量水充分反应转移的电子数目为0.2NA |
| C、1 mol碳的同位素中含有6NA个中子 |
| D、25 mL 16.0 mol?L-l浓盐酸与足量MnO2,加热反应,生成Cl2分子数目为0.1NA |
下列化学反应中属于氮的固定的是( )
A、N2+O2
| ||||
| B、O2+2NO=2NO2 | ||||
| C、H2O+3NO2═NO+2HNO3 | ||||
D、4NH3+5O2
|
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(OH-)>c(H+) |
| B、常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-) |
| C、常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7 mol?L-1 |
| D、物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-) |
在x R++yH++O2=m R2++nH2O离子反应方程式中,m值是( )
| A、2x | B、4 | C、3 | D、2 |