题目内容
17.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.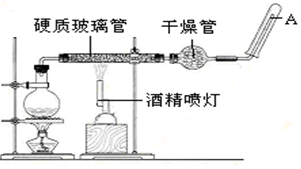
请回答该实验中的问题.
(1)写出该反应的化学方程式3Fe+4H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(2)实验前必须对整套装置进行的操作是检验装置的气密性;
(3)酒精灯和酒精喷灯点燃的顺序是先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯,为什么?防止先点燃酒精喷灯导致Fe与O2的反应.
(4)干燥管中盛装是的物质是碱石灰,作用是除去反应产生的H2中的水蒸气.
(5)试管中收集气体是氢气,如果要在A处玻璃管处点燃该气体,则必须对该气体进行验纯,这一操作的目的是防止点燃时,氢气因含有氧气而爆炸.
分析 (1)生成物是四氧化三铁和氢气;
(2)实验前必须对整套装置进行气密性检查;
(3)如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;该装置先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯,防止先点燃酒精喷灯导致Fe与O2的反应.;
(4)干燥管内固体干燥剂一般用无水氯化钙或固体氢氧化钠和碱石灰等,要注意干燥剂不能和被干燥的物质反应;
(5)铁与水蒸气反应生成氢气;点燃氢气前一定要检验纯度,防止发生爆炸.
解答 解:(1)铁与水蒸气发生氧化还原反应,反应的化学方程式为:3Fe+4H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(2)装置气密性影响实验进程,所以实验前必须对整套装置进行气密性检查,
故答案为:检验装置的气密性;
(3)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,产生水蒸气后,排掉硬质玻璃管内空气,再点燃酒精喷灯,
故答案为:先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯;防止先点燃酒精喷灯导致Fe与O2的反应;
(4)收集干燥氢气,需要用干燥剂除去反应产生的H2中的水蒸气,氢气为中性气体,可以用碱石灰干燥,
故答案为:碱石灰;除去反应产生的H2中的水蒸气;
(5)铁与水蒸气的反应为:3Fe+4H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,所以收集的气体为氢气;氢气为易燃气体,纯度不足时会发生爆炸,所以点燃氢气前一定要检验纯度,防止发生爆炸,
故答案为:氢气;验纯;防止点燃时,氢气因含有氧气而爆炸.
点评 本题为铁及其化合物的性质实验,题目难度中等,注意掌握装置气密性的方法及检验气体纯度的方法,试题培养了学生的分析能力及化学实验能力.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)2CCH2CH3 |
| A. | NH4NO3溶液与氢氧化钠共热:H++OH-═H2O | |
| B. | NH3•H2O滴入AlCl3溶液产生沉淀:3OH-+Al3+═Al(OH)3↓ | |
| C. | NaOH溶液与NaHCO3溶液混合:OH-+H+═H2O | |
| D. | Al(OH)3固体溶于稀硫酸中:Al(OH)3+3H+═Al3++3H2O |
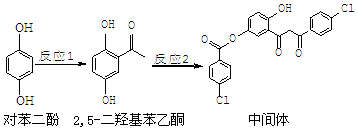
| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1 mol该中间体最多可与11 mol H2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、水解、缩聚反应 | |
| D. | 该中间体分子中含有羰基和烃基两种含氧官能团 |
 室温下,将0.10mol•L-1的盐酸滴入20mL0.10mol•L-1的氨水中,溶液的pH和pOH随加入盐酸体积变化的曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )
室温下,将0.10mol•L-1的盐酸滴入20mL0.10mol•L-1的氨水中,溶液的pH和pOH随加入盐酸体积变化的曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )| A. | M点所示的溶液中c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| B. | Q点所示的溶液中c(NH4+)>c(Cl-)>c(H+)=c(OH-) | |
| C. | N点所示的溶液中c(NH4+)=c(Cl-) | |
| D. | M点和N点所示的溶液中水的电离程度相同 |
| 选项 | 实验目的 | 实验方案 |
| A | 证明氧化性:H2O2比Fe3+强 | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| B | 鉴别KBr溶液和KI溶液 | 分别加入新制氯水,再加入CCl4振荡、静置,观察 |
| C | 配制100mL 1.0mol•L-1 CuSO4溶液 | 将25g CuSO4•5H2O溶于100mL蒸馏水中 |
| D | 除去CuO中混有的Al2O3 | 加入过量盐酸溶液后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 标准状况下,22.4L C2H4与C3H6混合气体所含有分子数为NA | |
| B. | 1L 0.1mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 1mol Na2O2与足量的CO2反应转移的电子数为2NA | |
| D. | 18g NH4+所含的电子数11NA |
| A. | c(H+)=0.1 mol•L-1的溶液:Na+、NH4+、SO42-、S2O32- | |
| B. | 使pH试纸显蓝色的溶液:Cu2+、NO3-、Fe3+、SO42- | |
| C. | 与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42- | |
| D. | 常温下$\frac{c({H}^{-})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |