题目内容
在标准状况下,336mL某气体的质量为1.065g。试计算该气体的相对分子质量。
71
【解析】
试题分析:336mL=0.336L,气体的物质的量为:n=V÷22.4L/mol=0.336L÷22.4L/mol得:
n=0.015mol,M=m/n=1.065g ÷0.015mol =71g/mol得M=71g/mol ,1mol任何粒子或物质的摩尔质量在以g/mol 为单位时,其数值与该粒子的相对原子质量或相对分子质量相等,故此气体的相对分子质量为71。
考点:有关物质的量的计算。

练习册系列答案
相关题目

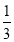 体积的自来水,并放入几粒沸石
体积的自来水,并放入几粒沸石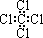 D.苯的分子式
D.苯的分子式