题目内容
写出下列物质在水溶液中的电离方程式:
NaOH ,K2SO4 ,KNO3 .
NaOH
考点:电离方程式的书写
专题:
分析:分清电解质的强弱,强电解质在水溶液里完全电离生成阴阳离子,电离方程式写“=”,弱电解质在水溶液里部分电离,电离方程式写“?”,书写时要遵循原子守恒、电荷守恒,据此分析解答.
解答:
解:(1)氢氧化钠是强碱,为强电解质,完全电离,电离方程式为:NaOH=Na++OH-,
故答案为:NaOH=Na++OH-;
(2)硫酸钾是盐,为强电解质,完全电离,电离方程式为:K2SO4=2K++SO42-,
故答案为:K2SO4=2K++SO42-;
(3)硝酸钾是盐,为强电解质,完全电离,电离方程式为:KNO3=K++NO3-,
故答案为:KNO3=K++NO3-.
故答案为:NaOH=Na++OH-;
(2)硫酸钾是盐,为强电解质,完全电离,电离方程式为:K2SO4=2K++SO42-,
故答案为:K2SO4=2K++SO42-;
(3)硝酸钾是盐,为强电解质,完全电离,电离方程式为:KNO3=K++NO3-,
故答案为:KNO3=K++NO3-.
点评:本题主要考查学生电离方程式的书写知识,明确电解质的强弱是解题关键,注意原子团不能拆.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列有关0.1mol/LNaOH 溶液的叙述正确的是( )
| A、该溶液中含有NaOH4g |
| B、100ml该溶液中含有Na+0.01mol |
| C、从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol/L |
| D、在1L水中溶解4g NaOH即可配制得0.1 mol/L NaOH溶液 |
下列离子方程式正确的是( )
| A、Al(OH)3滴加稀盐酸:OH-+H+=H2O |
| B、Fe片浸泡在FeCl3溶液中:Fe3++Fe=2Fe2+ |
| C、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
| D、MgCl2溶液中滴加氨水:Mg2++2OH-=Mg(OH)2↓ |
25℃时,弱酸的电离平衡常数如表所示,下列离子反应方程式错误的是( )
| 弱酸 | H2SO3 | HClO | H2CO3 |
| Ka1 | 1.54×10-2 | 2.95×10-8 | 4.30×10-7 |
| Ka2 | 1.02×10-7 | 5.61×10-11 |
| A、氯水中加入少量NaHCO3粉末:HCO3-+H+=H2O+CO2↑ |
| B、NaAl(OH)4溶液中通入足量的CO2:Al(OH)4-+CO2=Al(OH)3↓+HCO3- |
| C、NaClO溶液中通入少量CO2:2ClO-+H2O+CO2=CO32-+2HClO |
| D、Na2CO3溶液中通入少量SO2:2 CO32-+H2O+SO2=SO32-+2HCO3- |
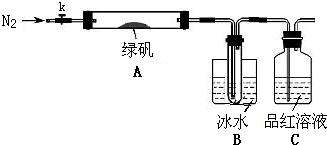 某学习小组拟通过实验探究绿矾(FeSO4?7H2O)热分解的产物.
某学习小组拟通过实验探究绿矾(FeSO4?7H2O)热分解的产物.