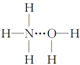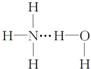题目内容
16.下列说法正确的是( )| A. | 向CH3CH2Br中滴入AgNO3溶液以检验溴元素 | |
| B. | 检验某卤代烃中是否含溴:加入NaOH溶液,加热,冷却,再加入硝酸银溶液 | |
| C. | 苯不能与溴水发生取代反应,用苯能萃取溴的四氯化碳溶液中的溴 | |
| D. | 利用核磁共振氢谱,可以鉴别CH3OCH3和CH3CH2OH |
分析 A.溴乙烷中没有自由移动溴离子,不能和硝酸银反应;
B.在加入硝酸银溶液之前必须加入稀硝酸中和未反应的NaOH;
C.苯不和溴水发生取代反应,苯、溴和四氯化碳互溶;
D.核磁共振氢谱检验氢原子种类,只要有机物中氢原子种类不同,可以用 核磁共振氢谱鉴别.
解答 解:A.溴乙烷中没有自由移动溴离子,不能和硝酸银反应,要检验溴乙烷中的溴元素,应该先将溴乙烷中溴元素转化为溴离子,然后再用硝酸银检验,故A错误;
B.在加入硝酸银溶液之前必须加入稀硝酸中和未反应的NaOH,否则硝酸银和NaOH反应而干扰实验目的,故B错误;
C.苯不和溴水发生取代反应,苯、溴和四氯化碳互溶,所以苯不能萃取溴的四氯化碳中的溴,故C错误;
D.核磁共振氢谱检验氢原子种类,只要有机物中氢原子种类不同,可以用核磁共振氢谱鉴别,这两种有机物中氢原子种类不同,所以可以用核磁共振氢谱鉴别,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及有机物鉴别、官能团检验、元素检验、萃取等知识点,明确实验原理、物质性质差异、实验基本操作等是解本题关键,注意B为易错点,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
6.下列离子方程式正确的是( )
| A. | 向碳酸氢钠溶液中滴入过量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO | |
| C. | 在KHSO4溶液中加入少量氢氧化钡溶液:Ba2++SO42-═BaSO4↓ | |
| D. | 向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3 SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
11.将m g的镁、铜合金加到一定量的稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后溶液中加入5mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金质量增加10.2g,则下列叙述正确的是( )
| A. | 当金属全部溶解时,无法计算出参与反应的硝酸的物质的量 | |
| B. | 7.2<m<19.2 | |
| C. | 当金属全部溶解时,收集到NO气体的体积一定为4.48L | |
| D. | 当生成沉淀的量达到最大值时,消耗NaOH溶液的体积为120mL |
8.“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用.它的有效成分与漂白液中的有效成分相同,这种物质是( )
| A. | KMnO4 | B. | NaClO | C. | Ca(ClO)2 | D. | HNO3 |
6.某溶液中若加入KSCN溶液出现血红色,则该熔液中可能大量存在的离子组是( )
| A. | Na+、K+、S2-、Cl- | B. | H+、Na+、I-、NH${\;}_{4}^{+}$ | ||
| C. | K+、Ba2+、OH-、NO${\;}_{3}^{-}$ | D. | Na+、Cl-、SO${\;}_{4}^{2-}$、Fe2+ |
 其含有的共价键类型是极性共价键.
其含有的共价键类型是极性共价键.