题目内容
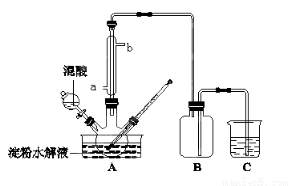
电石中的碳化钙和水能完全反应: CaC2+2H2O=C2H2↑+Ca(OH)2,使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置:
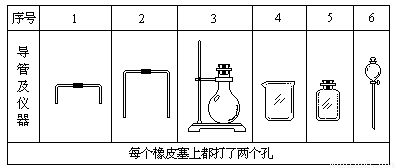
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:( )接( )接( )接( )接( )接( )。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。
(3)若实验产生的气体有难闻的臭鸡蛋这是因为含有 杂质。检验此杂质的反应为 。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是 %。
(1)6→3→1→5→2→4 (3分)
(2)②①③⑤④或①③②⑤④(3分)
(3)H2S(2分)H2S+CUSO4=CUS↓+H2SO4(2分)
(4)80(3分)
【解析】
试题分析:(1)该实验用排水量气法测量生成的乙炔的体积,所以选择1导气管导出气体,排出的水用导气管2。根据气体发生装置→收集装置,所以装置连接顺序是6→3→1→5→2→4;
(2)反应开始前应检查装置的气密性,再称取固体,装药品,开始实验,测量数据;前两步可颠倒,所以正确的操作顺序是②①③⑤④或①③②⑤④;
(3)具有臭鸡蛋气味的气体是H2S,该气体与硫酸铜溶液反应生成生成黑色沉淀,可证明该气体的存在,化学方程式为H2S+CUSO4=CUS↓+H2SO4
(4)乙炔的物质的量可计算出0.448L/22.4L/mol=0.02mol,所以碳化钙的物质的量为0.02mol,则质量为0.02mol×64g/mol=1.28g,,此电石中碳化钙的质量分数是1.28g/1.60g×100%=80%.
考点:考查实验装置的连接,步骤的判断,杂质的判断,质量分数的计算,化学方程式的书写

 作业辅导系列答案
作业辅导系列答案