题目内容
NA表示阿伏加德罗常数.下列说法正确的是( )
| A、0.1mol Na2O2中含有的阴离子数目为0.2NA |
| B、标准状况下,2.24L CHCl3的分子数为0.1NA |
| C、标准状况下,2.24L CHCl3的分子数为0.1NA |
| D、9.2g NO2和N2O4的混合气体中含有的氮原子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、过氧化钠是钠离子和过氧根离子构成;
B、CHCl3在标准状况不是气体;
C、CHCl3在标准状况不是气体;
D、NO2和N2O4的最简式相同为NO2,只需计算9.2g NO2中所含氮原子数;
B、CHCl3在标准状况不是气体;
C、CHCl3在标准状况不是气体;
D、NO2和N2O4的最简式相同为NO2,只需计算9.2g NO2中所含氮原子数;
解答:
解:A、过氧化钠是钠离子和过氧根离子构成,0.1mol Na2O2中含有的阴离子数目为0.1NA,故A错误;
B、CHCl3在标准状况不是气体,2.24L CHCl3的物质的量不是0.1mol,故B错误;
C、CHCl3在标准状况不是气体,2.24L CHCl3的物质的量不是0.1mol,故C错误;
D、NO2和N2O4的最简式相同为NO2,只需计算9.2g NO2中所含氮原子数=
×1×NA=0.2NA,故D正确;
故选D.
B、CHCl3在标准状况不是气体,2.24L CHCl3的物质的量不是0.1mol,故B错误;
C、CHCl3在标准状况不是气体,2.24L CHCl3的物质的量不是0.1mol,故C错误;
D、NO2和N2O4的最简式相同为NO2,只需计算9.2g NO2中所含氮原子数=
| 9.2g |
| 46g/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要是物质结构分析,气体摩尔体积的条件应用,掌握基础上是关键,题目较简单.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
如表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A、W元素的氢化物分子间有氢键 |
| B、Z和X能以共价键结合形成一种无机非金属材料 |
| C、Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 |
| D、X元素的非金属性比Y元素非金属性强 |
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),下列说法错误的是( )
| A、相同条件下,MnS的Ksp比CuS的Ksp大 | ||
B、该反应的平衡常数K=
| ||
| C、该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| D、往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 |
短周期元素中,X元素的阳离子和Y元素的阴离子具有相同的核外电子排布,下列叙述正确的是( )
| A、原子序数X<Y |
| B、原子半径X<Y |
| C、电子层数X=Y |
| D、离子半径X<Y |
用如图所示实验装置进行相应实验,能达到实验目的是( ) 

| A、装置①所示的气流方向可用于收集H2、NH3等 |
| B、按装置②可证明非金属性Cl>C>Si |
| C、装置③向左推动针筒活塞可检验该装置的气密性 |
| D、装置④可用于除去Cl2中含有的少量HCl气体 |
下列离子方程式正确的是( )
| A、锌粉与稀硝酸反应:Zn+2H+═Zn2++H2↑ | ||||
B、硫酸铵中NH4+的检验:NH4++OH-
| ||||
| C、NH4Al(SO4)2溶液与足量Ba(OH)2溶液混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
D、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
|
对下列说法不正确的是( )
| A、光化学烟雾的主要成分为氮的氧化物和碳氢化合物 |
| B、工业上可以从石油裂解气中获得乙烯 |
C、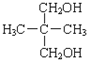 和 和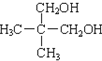 互为同分异构体 互为同分异构体 |
D、按系统命名法,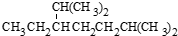 的名称为2,6-二甲基-3-乙基庚烷 的名称为2,6-二甲基-3-乙基庚烷 |
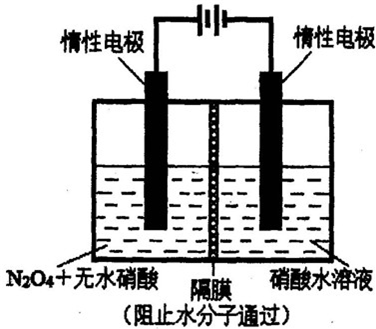 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.