题目内容
下列有关物质的结构或性质的叙述错误的是( )
| A、水是一种非常稳定的化合物,这是由于氢键所致 |
| B、由极性键形成的分子不一定是极性分子 |
| C、H2O、HF、NH3、CH4的沸点依次降低 |
| D、分子晶体中一定存在分子间作用力,可能有共价键 |
考点:含有氢键的物质
专题:化学键与晶体结构
分析:A、水中含有氢键,会导致其物理性质发生变化;
B、由极性键形成的分子如果是完全对称的结构的物质属于非极性分子;
C、H2O、HF、NH3分子间均存在氢键;
D、分子晶体中一定存在分子间作用力,但是其中可能含有共价键,可能没有.
B、由极性键形成的分子如果是完全对称的结构的物质属于非极性分子;
C、H2O、HF、NH3分子间均存在氢键;
D、分子晶体中一定存在分子间作用力,但是其中可能含有共价键,可能没有.
解答:
解:A、是一种非常稳定的化合物,属于化学性质的表现,其中含有氢键,会导致沸点较高,和性质稳定无关,故A错误;
B、由极性键形成的分子不一定是极性分子,如甲烷,是由极性键形成的分子,是非极性分子,故B正确;
C、H2O、HF、NH3分子间均存在氢键,H2O、HF、NH3的沸点高于CH4,H2O、HF、NH3、CH4的沸点依次降低,故C正确;
D、分子晶体中一定存在分子间作用力,可能有共价键(如水分子),可能没有(如稀有气体分子),故D正确.
故选A.
B、由极性键形成的分子不一定是极性分子,如甲烷,是由极性键形成的分子,是非极性分子,故B正确;
C、H2O、HF、NH3分子间均存在氢键,H2O、HF、NH3的沸点高于CH4,H2O、HF、NH3、CH4的沸点依次降低,故C正确;
D、分子晶体中一定存在分子间作用力,可能有共价键(如水分子),可能没有(如稀有气体分子),故D正确.
故选A.
点评:本题是一道关于化学键和分子结构知识的考查题,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
相关题目
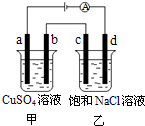 如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )
如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )| A、乙烧杯中d的电极反应为 2Cl--2e-═Cl2↑ |
| B、a、c两极产生气体的物质的量相等 |
| C、甲、乙两烧杯中溶液的pH均保持不变 |
| D、乙烧杯中通入适量HCl气体,溶液组成可以恢复 |
符合下列分子式的有机物,没有同分异构现象的是( )
| A、C4H10 |
| B、C12H22O11 |
| C、C3H8 |
| D、C4H8 |
如图所示的装置,有关说法正确的是( )
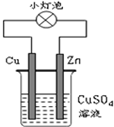

| A、电子由Cu流向Zn |
| B、Cu是正极,发生氧化反应 |
| C、溶液中Cu2+向Cu电极移动 |
| D、Cu在Zn电极上析出 |
在标准状况下,称量一个充满Cl2的容器质量为74.6g,若改充氮气,其质量为66g,则容器充满SO2气体时的质量为( )
| A、64.8 g |
| B、73.2 g |
| C、68.6 g |
| D、75.8 g |
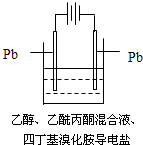 有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:2CH3CH2OH+2e-=2CH3CH2O-+H2↑
2CH3COCH2COCH3+2e-=2(CH3COCHCOCH3)+H2↑
下列说法正确的是( )
| A、阳极Pb失去电子,发生还原反应 |
| B、当阳极失去2 mol e-时,阴极产生2 mol氢气 |
| C、电解过程中,阳离子向阴极移动 |
| D、已知Pb-4e-=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol |
下列变化或数据与氢键无关的是( )
| A、冰的密度比水的密度小 |
| B、氨极易溶于水 |
| C、苯酚溶于热水 |
| D、SbH3的沸点比PH3高 |
某原电池装置如图所示.下列说法正确的是( )
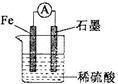

| A、石墨棒为负极 |
| B、铁片的质量减少 |
| C、硫酸被氧化 |
| D、电子从石墨棒流向铁片 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、18g D2O含有的电子数为10NA |
| B、1mol Na2O2与水完全反应时转移电子数为2NA |
| C、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| D、200mL1mol/LFe2(SO4)3溶液中,Fe3+和SO42-离子数的总和是NA |