题目内容
在pH=1的无色溶液中能大量共存的离子组是( )
| A、K+、Cr2O72-、SO42-、NO3- |
| B、Na+、K+、SO42-、Cl- |
| C、Na+、Ca2+、HCO3-、Cl- |
| D、Na+、Ba2+、Cl-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:pH=1的溶液中含有大量的H+,离子之间不能结合水、气体、沉淀、弱电解质,不能发生氧化还原反应等,则离子能大量共存,并注意离子的颜色,以此来解答.
解答:
解:A.Cr2O72-有颜色,不符合题目无色要求,故A错误;
B.溶液无色,且在酸性条件下不发生任何反应,可大量共存,故B正确;
C.酸性条件下,HCO3-不能大量共存,故C错误;
D.Ba2+与SO42-反应生成沉淀而不能大量共存,故D错误.
故选B.
B.溶液无色,且在酸性条件下不发生任何反应,可大量共存,故B正确;
C.酸性条件下,HCO3-不能大量共存,故C错误;
D.Ba2+与SO42-反应生成沉淀而不能大量共存,故D错误.
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应的考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
下列事实(常温下)不能说明醋酸是弱电解质的是( )
| A、醋酸钠溶液pH>7 |
| B、醋酸溶液能溶解碳酸钙 |
| C、0.1mol?L-1醋酸溶液pH=2.9 |
| D、pH=1的醋酸溶液稀释100倍后pH<3 |
在由水电离出的c(H+)=1×10-13 mol/L的溶液中,一定可以大量共存的是( )
| A、Ba2+ Na+ NO3- Cl- |
| B、Fe2+ Na+ NO3- Cl- |
| C、SO42- S2O32- NH4+ Na+ |
| D、Mg2+ Na+ Br- AlO2- |
 常温下,浓度均为0.1000mol?L-1的三种一元酸HX、HY、HZ,分别用0.1000mol?L-1的NaOH溶液进行滴定,滴定曲线如图所示.下列有关叙述正确的是( )
常温下,浓度均为0.1000mol?L-1的三种一元酸HX、HY、HZ,分别用0.1000mol?L-1的NaOH溶液进行滴定,滴定曲线如图所示.下列有关叙述正确的是( )| A、NaOH溶液与三种酸的反应均是吸热反应 |
| B、滴定酸HY可用酚酞作指示剂 |
| C、酸性强弱:HX>HY>HZ |
| D、滴定三种酸都可用甲基橙作指示剂 |
短周期元素A、B、C,D、E原子序数依次增大,其中A、C同主族,B、E同主族,A的最外层电子数与次外层电子数相等,E是太阳能转化为电能的常用材料,则下列说法正确的是( )
| A、最价氧化物对应水化物碱性强弱:A>C |
| B、C、D的简单阳离子均可促进水的电离 |
| C、B、E的最高价氧化物具有相似的物理性质和化学性质 |
| D、含D的盐溶于水一定显酸性 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Cl2与过量的镁铁反应,转移2NA个电子 |
| B、常温下,16g CH4含有8NA个电子 |
| C、1L 0.5mol?L-1 Na2SO4溶液中含有NA个SO42- |
| D、常温常压下,22.4L CO2含有NA个CO2分子 |
人类社会需要科学发展.下列做法科学合理的是( )
| A、在田间焚烧秸秆,增加草木灰肥料 |
| B、大量开采地下水,以满足生产、生活的需求 |
| C、用“复合石头纸”替代木浆纸,减少树木砍伐 |
| D、尽可能多的使用各种添加剂,改善食品的品质 |
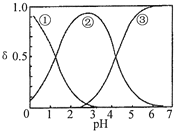 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )| A、曲线①代表的粒子是HC2O4- |
| B、0.1 mol?L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| C、pH=5时,溶液中主要含碳物种浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) |
| D、一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)不变 |
 试回答:
试回答: