��Ŀ����
13��ij�о���ѧϰС�������CO2������ȼ�ս���������ʵ�飺| �������� | ʵ������ |
| �����﴿����CO2����ͨ�������Ƶ����ž������ĸ��ﲣ�����У����� | ��ȼ�գ�����Ϊ��ɫ |
| ��Ӧ����ȴ | �ܱڸ��к�ɫ�����Ͱ�ɫ���� |
��ɫ���ʿ�����Na2O��
��ɫ���ʿ�����Na2CO3
��ɫ���ʻ�������Na2O��Na2CO3�����
��2��Ϊȷ���ð�ɫ���ʵijɷ֣���С�����������ʵ�飺
| ʵ�鲽�� | ʵ������ |
| ��������ɫ�������Թ��У���������ˮ������Ʒȫ������ˮ�������мӹ�����CaC12��Һ���ְ�ɫ���� | ���ְ�ɫ���� |
| �ھ���Ƭ�̣�ȡ�ϲ���Һ���Թ��У��μ���ɫ��̪��Һ | ���������� |
��������CO2��ȼ�յĻ�ѧ����ʽΪ4Na+3CO2$\frac{\underline{\;��ȼ\;}}{\;}$2Na2CO3+C��
�۱�ͬѧ��Ϊ��ɫ�����п������������ƣ�����Ϊ�Ƿ������˵�����ɲ���ȷ����Ϊ��Ӧ������HԪ�أ���Υ�������غ㶨�ɣ���
��3����ͬѧ��ȡNa2O��Ʒmg������ֻ����Na2O2���ʣ���������������������ѡ�ú��ʵ��������Լ������һ�ֿ�ѡ�õ�ʵ��������ϣ���д�±��������Ʒ��Na2O�����IJⶨ����ѡ�õ��Լ���
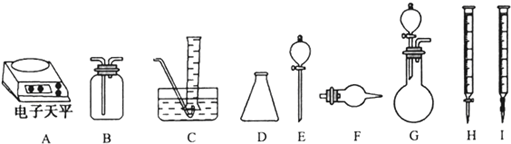
a��Ũ���� b��ˮ c���������Һ d��NaOH ����Һ e����̪ f����ʯ�� g��ϡ����
| ʵ������з�����Ӧ�Ļ�ѧ����ʽ | ʵ����������������ĸ��ʾ�� | ʵ�������Լ������ֱ�ʾ�� | ʵ����ֱ�Ӳⶨ���й���������������˵���� |
7.75gNa2O��Ʒ$\stackrel{�������г������}{��}$����$\stackrel{��ȴ}{��}$�����ù���9.35g����Na2O��Ʒ��Na2O����������Ϊ80%��
���� ��1����ɫ���廹��������������̼���ƵĻ���
��2��������������ˮ��Ӧ�����������ƣ��������Ʋ������Ȼ��Ʒ�Ӧ��
�����ݷ����٢ڵķ�Ӧ����ͽ��ۣ��������ƶ����ڶ�����̼��ȼ������̼���ƺ�̼��
�����ݷ�Ӧ���е�Ԫ���غ�����ж�����������Ԫ�أ�
��3����ȡNa2O��Ʒmg������ֻ����Na2O2���ʣ��������Ʒ��Na2O�����IJⶨ�����Գ�ȡ��Ʒ������D�У�ͨ������ˮ��Ӧ��ȫ�ⶨ��Ӧǰ����ƿ�������õ��ų�������������ϻ�ѧ����ʽ������ϵ����������������õ�������������������ѡ��GCװ�ã�һ��������Ʒ�е���ˮ��Ӧ��ⶨ�����������������Ϊ��״������õ������������ݻ�ѧ����ʽ������ϵ����õ����������������õ����������������������ñ�������Һ�ζ���Ӧ����Һ�����ɵ��������Ƶ��������Ԫ���غ���ʽ����õ������ƺ������Ƶ��������õ�����������������
��4��7.75g��Ʒ�ڿ����г�����յõ��������ƣ���ȴ������������9.35g����ϻ�ѧ����ʽ������ϵ��������������������
��� �⣺��1�����ڶ�����̼��ȼ����һ��ѧ��Ӧ�ķ�Ӧ����ֻ������Ԫ�ء�̼Ԫ�غ���Ԫ�أ�û����Ԫ�أ��������������ƻ�̼���ƻ���ߵĻ���
�ʴ�Ϊ��Na2O��Na2CO3�Ļ���
��2��������������ˮ��Ӧ�����������ƣ��������Ʋ������Ȼ�����Һ��Ӧ������ɫ����������ˮ��Һ�Լ��ԣ�̼���������Ȼ��Ʒ�Ӧ�����Ȼ��ƺ�̼��ư�ɫ�������ʢ�������ʴ�Ϊ����
�����������ʵ������ж����ڶ�����̼������ȼ������̼���ƺ�̼���ʣ���Ӧ�Ļ�ѧ����ʽΪ��4Na+3CO2$\frac{\underline{\;��ȼ\;}}{\;}$2Na2CO3+C��
�ʴ�Ϊ��4Na+3CO2$\frac{\underline{\;��ȼ\;}}{\;}$2Na2CO3+C��
�۱�ͬѧ��Ϊ��ɫ�����п������������ƣ��Ǵ���ģ��ڷ�Ӧ�����У������ڶ�����̼������ ��ȼ�շ�Ӧ������Ԫ�صĴ��ڣ�ʵ������Ԫ���غ���û������������������ƣ�
�ʴ�Ϊ������ȷ����Ϊ��Ӧ������HԪ�أ���Υ�������غ㶨�ɣ���
��3����ȡNa2O��Ʒmg������ֻ����Na2O2���ʣ��������Ʒ��Na2O�����IJⶨ�����Գ�ȡ��Ʒ������D�У�ͨ������ˮ��Ӧ��ȫ�ⶨ��Ӧǰ����ƿ�������õ��ų�������������ϻ�ѧ����ʽ������ϵ����������������õ�������������������ѡ��GCװ�ã�һ��������Ʒ�е���ˮ��Ӧ��ⶨ�����������������Ϊ��״������õ������������ݻ�ѧ����ʽ������ϵ����õ����������������õ����������������������ñ�������Һ�ζ���Ӧ����Һ�����ɵ��������Ƶ��������Ԫ���غ���ʽ����õ������ƺ������Ƶ��������õ�����������������ʵ������з�����Ӧ�Ļ�ѧ����ʽ��ʵ������������ʵ�������Լ���ʵ����ֱ�Ӳⶨ���й������������ʾ��
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH | A��D | b | �ٷ�Ӧǰ��ƿ����Ʒ��ˮ�������� �ڷ�Ӧ����ƿ����Һ�������� |
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH | G��C | b | ��Ͳ���ռ������������� |
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH�� NaOH+HCl=NaCl+H2O | D��H | b��c��e | �к���ƿ����Ʒ��ˮ��Ӧ��������Һʹ�õ��������Һ����� |
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH | A��D | b | �ٷ�Ӧǰ��ƿ����Ʒ��ˮ�������� �ڷ�Ӧ����ƿ����Һ�������� |
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH | G��C | b | ��Ͳ���ռ������������� |
| 2Na2O2+2H2O=4NaOH+O2���� Na2O+H2O=2NaOH�� NaOH+HCl=NaCl+H2O | D��H | b��c��e | �к���ƿ����Ʒ��ˮ��Ӧ��������Һʹ�õ��������Һ����� |
�ʴ�Ϊ��80%��
���� ���⿼�����ʵ����̽����Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ����������ѧ���ķ���������ʵ�������Ŀ��飬ע�����������ʵ��ۺ�Ӧ�ã����ݷ�Ӧ������ȷ�жϷ�Ӧ�����ǽ����Ĺؼ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | Mg2+/Mg | B�� | Cl/Cl- | C�� | N/O | D�� | Na+/F |
��2������Һ����SO2�Ĺ����У�pH��n ��SO32-����n��HSO3-���仯��ϵ���±���
| n��SO₃2-������n��HSO₃-�� | 91��9 | 1��1 | 1��91 |
| PH | 8.2 | 7.2 | 6.2 |
������Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ���ǣ�ѡ����ĸ����ab
a��c��Na+��=2c��SO32-��+c��HSO3-��
b��c��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-��
c��c��Na+��+c��H+��=c��SO32-��+c��HSO3-��+c��OH-��
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | ���� |
| A�� | 0.8mol•L-1 | B�� | 0.6mol•L-1 | C�� | 0.4mol•L-1 | D�� | 0.2mol•L-1 |
| ѡ�� | ��ѧʽ | ����ʽ���еĻ�ѧ������ | ���ʵ����� | ���������Ӧ����; |
| A | NaClO | ���Ӽ� ���ۼ� | ǿ������ | ������ |
| B | H2O2 | 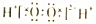 | ���ȶ����ֽ� | ҽ�������� |
| C | NH3 | ���ۼ� | ˮ��Һ�������� | ��ҵ������ |
| D | NaHCO3 | ���Ӽ� | �����ֽ� | ��ĭ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
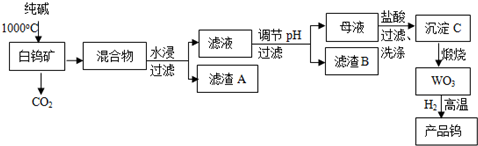

 ��
��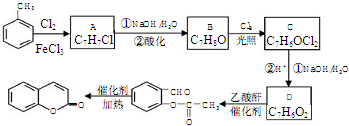
 ��A��B�ķ�Ӧ������ȡ����Ӧ��
��A��B�ķ�Ӧ������ȡ����Ӧ�� ����Ӧ��������
����Ӧ�������� �⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ��CH3COOH��
�⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ��CH3COOH�� ��Ϊͬ���칹�壬�Ҿ��������ص㣺
��Ϊͬ���칹�壬�Ҿ��������ص㣺 ��д��A�����й����ŵ������ǻ����Ȼ���
��д��A�����й����ŵ������ǻ����Ȼ��� ��
��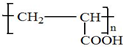 ��
��