题目内容
近年来,科学家合成了一系列具有独特化学特性的(AlH3)n氢铝化合物。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如图。下列有关说法肯定错误的是( )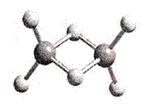
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |
D
解析试题分析:该化合物的熔点低,因此形成的晶体类型应该是分子晶体,A正确;该化合物的,燃烧热极高,所以选项B和C都是正确的;Al2H6中只含有极性共价键,不存在离子键,D不正确,答案选D。
考点:考查晶体类型、性质、以及化学键的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重考查学生基础知识的同时,侧重考查学生灵活运用基础知识解决实际问题的能力。有助于培养学生的逻辑推理能力和知识的迁移能力,提升学生的学科素养和学习兴趣。

练习册系列答案
相关题目
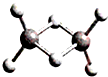 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、Al2H6在空气中完全燃烧,产物为氧化铝和水 | C、氢铝化合物可能成为未来的储氢材料和火箭燃料 | D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
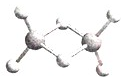 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、氢铝化合物可能成为未来的储氢材料和火箭燃料 | C、Al2H6在空气中完全燃烧,产物为氧化铝和水 | D、Al2H6中含有离子键和极性共价键 |
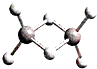 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A、Al2H6可以燃烧,产物为氧化铝和水 | B、1mol Al2H6中约含有4.8×1024个σ键 | C、60g Al2H6中含铝原子约为1.2×1023个 | D、Al2H6在固态时所形成的晶体是离子晶体 |
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量。Al2H6球棍模型如下图。下列说法肯定错误的是( )
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |
