题目内容
6.在密闭容器中,加入一定量的A、B混合气体,发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0,40mol/L,下列有关判断正确的是( )| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率降低 | D. | C的产率不变 |
分析 平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,如平衡不移动,则A的浓度应降低为0.4mol/L,而此时为0.4mol/L,则说明降低压强平衡向不发生移动,以此进行判断.
解答 解:平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,如平衡不移动,则A的浓度应降低为0.4mol/L,而此时为0.4mol/L,则说明降低压强平衡向不发生移动,证明反应前后气体体积不变的反应,
A.减小压强平衡不变,x+y=z,故A错误;
B.保持温度不变,将容器的容积扩大到原来的两倍,如平衡不移动,则A的浓度应降低为0.4mol/L,而此时为0.4mol/L,则说明降低压强平衡向不发生移动,故B错误;
C.平衡不变,B的转化率不变,故C错误;
D.分析可知改变容器体积,压强减小,平衡不变,所以C的产率不变,故D正确;
故选D.
点评 本题考查化学平衡移动知识,题目难度不大,注意从浓度的变化的角度判断平衡移动的方向,结合压强对平衡移动的影响分析.

练习册系列答案
相关题目
16.检验氯化氢气体中是否混有氯气,不可采用的方法是( )
| A. | 用湿润的有色布条 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 将气体通入硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
17.在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )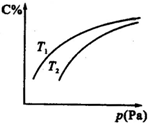

| A. | B一定为气体 | |
| B. | A一定为气体 | |
| C. | 若正反应方向△H<0,则T1>T2 | |
| D. | 压强增大时,混合气体的平均相对分子质量减小 |
14.有八种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯⑧环己烯,既能使KMnO4酸性溶液褪色,又能与溴水反应使之褪色的是( )
| A. | ①④⑤⑧ | B. | ②④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
18.在无色溶液中能大量共存的离子组是( )
| A. | Na+H+ AlO2- SO32- | B. | NH4+ Al3+SO42-Cl- | ||
| C. | OH- K+ SO42- HCO3- | D. | Fe2+Na+ ClO-NO3- |
15.下列说法不正确的是( )
| A. | 碳酸钠不能用于治疗胃溃疡病人的胃酸过多症 | |
| B. | 切开的金属Na暴露在空气中,光亮表面会逐渐变暗 | |
| C. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| D. | 金属镁在空气中燃烧的产物是纯净的氧化镁 |
16.下列物质中,含有离子键和共价键的是( )
| A. | HCl | B. | MgO | C. | NaCl | D. | NaOH |