题目内容
已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2
2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.

回答下列问题:
(1)B、D分子中的官能团名称分别是 、 .
(2)写出下列反应的反应类型:① ,② ,④ .
(3)写出下列反应的化学方程式:
① ;② ;④ .
| 催化剂 |
| △ |

回答下列问题:
(1)B、D分子中的官能团名称分别是
(2)写出下列反应的反应类型:①
(3)写出下列反应的化学方程式:
①
考点:乙烯的化学性质,有机物的推断
专题:有机物的化学性质及推断
分析:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,与水发生加成反应生成CH3CH2OH,乙醇氧化生成CH3CHO,CH3CHO进一步氧化可得CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成CH3COOCH2CH3,结合有机物的结构和性质解答该题.
解答:
解:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,与水发生加成反应生成
CH3CH2OH,乙醇氧化生成CH3CHO,CH3CHO进一步氧化可得CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成CH3COOCH2CH3,则
(1)由以上分析可知B为CH3CH2OH,D为CH3COOH,分别含有羟基和羧基,故答案为:羟基、羧基;
(2)A为CH2=CH2,与水发生加成反应生成CH3CH2OH,②为乙醇的氧化反应,④为乙酸和乙醇的酯化反应,
故答案为:加成;氧化;酯化(取代);
(3)①CH2=CH2与水发生加成反应生成CH3CH2OH,化学方程式为:CH2=CH2+H2O
CH3CH2OH,
故答案为:CH2=CH2+H2O
CH3CH2OH;
②乙醇在Cu或Ag作催化剂,加热条件下被氧化生成CH3CHO,反应的化学方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;
③CH3COOH与CH3CH2OH在浓硫酸作用下加热发生酯化反应生成CH3COOCH2CH3,
反应的化学方程式为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O.
CH3CH2OH,乙醇氧化生成CH3CHO,CH3CHO进一步氧化可得CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成CH3COOCH2CH3,则
(1)由以上分析可知B为CH3CH2OH,D为CH3COOH,分别含有羟基和羧基,故答案为:羟基、羧基;
(2)A为CH2=CH2,与水发生加成反应生成CH3CH2OH,②为乙醇的氧化反应,④为乙酸和乙醇的酯化反应,
故答案为:加成;氧化;酯化(取代);
(3)①CH2=CH2与水发生加成反应生成CH3CH2OH,化学方程式为:CH2=CH2+H2O
| 一定条件 |
故答案为:CH2=CH2+H2O
| 一定条件 |
②乙醇在Cu或Ag作催化剂,加热条件下被氧化生成CH3CHO,反应的化学方程式为2CH3CH2OH+O2
| Cu |
| △ |
| Cu |
| △ |
③CH3COOH与CH3CH2OH在浓硫酸作用下加热发生酯化反应生成CH3COOCH2CH3,
反应的化学方程式为CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
点评:本题考查有机物的合成,题目难度不大,注意常见有机物的性质即可解答该题,掌握有机物的官能团变化为解题的关键.

练习册系列答案
相关题目
下列有关物质性质实验的叙述,正确的是( )
| A、钠在空气中燃烧,生成淡黄色的氧化钠粉末 |
| B、镁在CO2中燃烧,生成白色的氧化镁和黑色的碳 |
| C、将灼热的铁丝放入盛有氯气的集气瓶中,生成棕黄色的氯化铁烟雾 |
| D、在铜和浓硫酸加热反应后的混合液中加水,得到无色硫酸铜溶液 |
对于可逆反应2SO2+O2?2SO3达到平衡的标志是( )
| A、SO2、O2、SO3的物质的量浓度不再变化 |
| B、O2和SO3的化学反应速率相等 |
| C、SO2、O2、SO3的分子数之比为2:1:2 |
| D、单位时间生成2n mol SO2,同时生成n mol O2 |
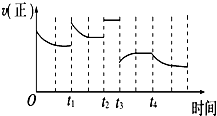 合成氨反应:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如图,下列说法正确的是( )
合成氨反应:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如图,下列说法正确的是( )| A、t1时升高了温度 |
| B、t2时使用了催化剂 |
| C、t3时降低了温度 |
| D、t4时减小了压强 |
称取两份铝粉,第一份加足量的氢氧化钠溶液,第二份加足量盐酸,如要放出等体积的气体(同温、同压下),两份铝粉的质量之比为( )
| A、1:2 | B、1:3 |
| C、3:2 | D、1:1 |
一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Zn | Cu | CuCl2 |
| B | Zn | Cu | ZnCl2 |
| C | Cu | Zn | CuSO4 |
| D | Cu | Zn | ZnSO4 |
| A、A | B、B | C、C | D、D |
下列溶液中的氯离子浓度与50mL 1mol/L的AlCl3溶液中氯离子浓度相等的是( )
| A、50 mL 1 mol/L的NaCl |
| B、100 mL 3 mol/L的NH4Cl |
| C、75 mL 2 mol/L的KCl |
| D、75 mL 2 mol/L的CaCl2 |
 由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁. 和
和 ;③氧气(O2)与臭氧(O3);④D与T;
;③氧气(O2)与臭氧(O3);④D与T;
