��Ŀ����
20��������ع㷺������ҵ�����е���������ҽ����ҵ�еķ�����������������������Ư����ˮ�ʾ�������ˮ�����е�ˮ�������ȣ��ش�����������⣺��1�������ʷ��������������������bce������ţ���
a���� b���� c�������d���ǵ���� e��������
��2���������ˮ��Һ�ܵ��磬��ԭ����KMnO4=K++MnO4-���û�ѧ�����ʾ����
��3��ʵ�����Ѕ�������ش���Mn02��Ũ�����ڲ����ȵ��������Ʊ�Cl2���÷�Ӧ�����ӷ���ʽΪ2MnO4-+10Cl-+16H+=5Cl2��+2Mn2++8H2O���÷�Ӧ�У�Ũ��������������ԡ���ԭ�ԣ�
��4��ҽ����ҵ�г��ø�����Ѻ��Һ����ᷴӦ��ԭ�����ⶨѪҺ�иƵĺ�������ƽ
�÷�Ӧ�����ӷ���ʽ��2Mn04-+5H2C204+6H+=CO2��+2 Mn2++8H2O��
���� ��1����������ǽ��������Ӻ���������ӹ��ɵĻ����ˮ��Һ�е������ڵ���ʣ�
��2���������ˮ��Һ�ܵ�������Ϊ�������ˮ��Һ�е���������ƶ������ӣ�
��3��������غ�Ũ���ᷴӦ������������Ӧ��Ũ������ʾ�����Ժͻ�ԭ�ԣ�
��4����Ԫ�ػ��ϼ�+7�۱仯Ϊ+2�ۣ�̼Ԫ�ػ��ϼ�+3�۱仯Ϊ+4�ۣ���ϵ����غ㡢ԭ���غ���ƽ��д���ӷ���ʽ��
��� �⣺��1����������ǽ��������Ӻ���������ӹ��ɵĻ����ˮ��Һ�е������ڵ���ʣ���ѡbce���ʴ�Ϊ��bce��
��2���������ˮ��Һ�ܵ��磬��ԭ����ˮ��Һ�е���������ƶ����ӵ��磬���뷽��ʽΪ��KMnO4=K++MnO4-���ʴ�Ϊ��KMnO4=K++MnO4-��
��3��ʵ�����Ѕ�������ش���Mn02��Ũ�����ڲ����ȵ��������Ʊ�Cl2����Ӧ�����ӷ���ʽΪ��2MnO4-+10Cl-+16H+=5Cl2��+2Mn2++8H2O����Ԫ�ػ��ϼ۱仯�������÷�Ӧ�У�Ũ��������������ԡ���ԭ�ԣ�
�ʴ�Ϊ��2MnO4-+10Cl-+16H+=5Cl2��+2Mn2++8H2O�����ԡ���ԭ�ԣ�
��4����Ԫ�ػ��ϼ�+7�۱仯Ϊ+2�ۣ�����ת��5��̼Ԫ�ػ��ϼ�+3�۱仯Ϊ+4�ۣ�����ת��1����ϵ����غ㡢ԭ���غ���ƽ��д���ӷ���ʽΪ��2Mn04-+5H2C204+6H+=10CO2��+2Mn2++8H2O��
�ʴ�Ϊ��2��5��6��10��2��8H2O��
���� ���⿼�������ʷ��ࡢ������ԭ��Ӧ�����ӷ���ʽ��д�����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ����ѹǿ��kPa�� | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| ƽ��������Ũ�� ����10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A��2v��NH3��=v��CO2��B���ܱ���������ѹǿ����
C���ܱ������л��������ܶȲ��� D���ܱ������а����������������
�ڸ��ݱ������ݣ���ʽ����25.0��ʱ�ķֽ�ƽ�ⳣ����K=1.6��10-8��mol•L-1��3��
�۰�������立ֽⷴӦ���ʱ��H��0���ر��S��0���������=����
��2����֪��NH2COONH4+2H2O?NH4HCO3+NH3•H2O�����о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨˮ�ⷴӦ���ʣ��õ�c��NH2COO-����ʱ��仯������ͼ��ʾ��

����25��ʱ��0��6min���������ˮ�ⷴӦ��ƽ������0.05mol/��L•min����
| A�� | K+��Cl-��NO3-��Fe2+ | B�� | K+��Mg2+��I-��SO42- | ||
| C�� | K+��Ca2+��Cl-��HCO3- | D�� | Na+��Cl-��NO3-��S042- |
| t/min | 2 | 4 | 7 | 9 |
| n��Y��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A�� | ���¶��´˷�Ӧ��ƽ�ⳣ��K=1.44 | |
| B�� | �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ�ͣ��棩���ͣ����� | |
| C�� | �����������䣬�ٳ���0.2molZ��ƽ��ʱX������������� | |
| D�� | 0��2min��ƽ�����ʦͣ�Z��=2.0��10-3mol•L-1•min-1 |
| A�� | 2gH2�е�ԭ����ĿΪNA | |
| B�� | 64gSO2�е�ԭ����ĿΪ3NA | |
| C�� | 1mol/LNaOH��Һ�е�Na+����ĿΪNA | |
| D�� | ���³��£�11.2LCl2�еķ�����ĿΪ0.5NA |
| A�� | n��H2CO3����c��HCO3-��֮��Ϊ1mol��NaHCO3��Һ�У�����Na+��ĿΪNA | |
| B�� | 5g 21H��31H�Ļ������Ⱥ˾۱䷴Ӧ��21H+31H��42He+10n�������������ӣ�10n����ΪNA | |
| C�� | 1L 0.1mol/L�Ҵ���Һ�д��ڵĹ��ۼ�����Ϊ0.8NA | |
| D�� | 56g ��������������Ӧ���������õ�3NA������ |

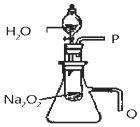 ʵ�鷨�ǻ�ѧ��Ҫ���о��������ʵĻ���������ij��ѧ�о�С�����������ʵ�飬��ش����⣮
ʵ�鷨�ǻ�ѧ��Ҫ���о��������ʵĻ���������ij��ѧ�о�С�����������ʵ�飬��ش����⣮