题目内容
(15分)
M、N、R、T为周期表中前四周期相邻两个周期的元素,且原子序数依次增大。已知T的次外层上电子没有排满,且该能层中成对电子数等于其它各能层上电子的总数;R和T在同一族;N的外围电子总数为6,均为未成对电子。根据以上信息,回答下列问题:
(1)T的元素符号为 ,在周期表中位于 族,N的价电子排布式为 。
(2)M和R两种元素组成的常见化合物有两种,其中一种可以单质之间进行化合,生成R的高价态化合物,请写出该反应的化学方程式: 。
(3)表面上附着氮原子的R可做为工业催化剂,下图为氮原子在R的晶面上的单层附着局部示意图(图中小黑色球代表氮原子, 灰色球代表R原子)。则图示颗粒表面上氮原子与R原子的个数比为 。

(4)T、N都有多种配合物,[T(NH3)3(H2O)M2]M是T配合物的一种,其中心离子的化合价为 ,配位数为 。N与甲基丙烯酸根的配合物为:
 该化合物中存在的化学键类型有
。甲基丙烯酸分子中C原子的杂化方式有
。
该化合物中存在的化学键类型有
。甲基丙烯酸分子中C原子的杂化方式有
。
【答案】
(15分)

【解析】

练习册系列答案
相关题目
R、M、T、G、J为原子序数依次递增的同一周期主族元素,下列说法一定正确的是(m、n均为正整数)( )
| A、若M(OH)n+1为强碱,则R(OH)n也为强碱 | B、若HnJOm为强酸,则G是位于ⅤA以后的活泼非金属元素 | C、若T的最低化合价为-3,则J的最高正化合价为+6 | D、若M的最高正化合价为+4,则五种元素都是非金属元素 |

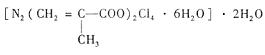 该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
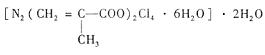 该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。