题目内容
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝的环境意义是 .
(2)选择性催化还原法的脱硝原理为:6NOx+4x NH3
(3+2x)N2+6xH2O
上述反应中每转移3mol电子,生成标准状况下N2的体积为 L.
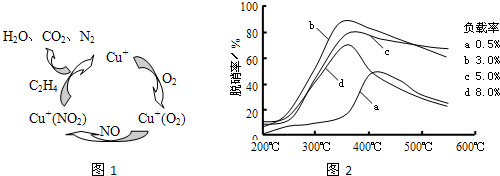
(3)目前,科学家正在研究一种以乙烯(C2H4)作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式: .
②为达到最佳脱硝效果,应采取的条件是 .
(1)烟气脱硫、脱硝的环境意义是
(2)选择性催化还原法的脱硝原理为:6NOx+4x NH3
| ||
上述反应中每转移3mol电子,生成标准状况下N2的体积为
(3)目前,科学家正在研究一种以乙烯(C2H4)作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.

①写出该脱硝原理总反应的化学方程式:
②为达到最佳脱硝效果,应采取的条件是
考点:氧化还原反应的计算,氮的氧化物的性质及其对环境的影响
专题:计算题,元素及其化合物
分析:(1)硫的氧化物、氮的氧化物是形成酸雨的主要成因,烟气脱硫、脱硝可以防止酸雨的发生;
(2)反应中氨气中的N元素由-3价升高为0价,据此计算转移3mol电子参加反应的氨气的物质的量,再根据方程式计算生成的氮气,根据V=nVm计算氮气的体积;
(3)①图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,据此写出反应的总方程式;
②为达到最佳脱硝效果,应满足脱硝率高,负载率低,适宜的温度.
(2)反应中氨气中的N元素由-3价升高为0价,据此计算转移3mol电子参加反应的氨气的物质的量,再根据方程式计算生成的氮气,根据V=nVm计算氮气的体积;
(3)①图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,据此写出反应的总方程式;
②为达到最佳脱硝效果,应满足脱硝率高,负载率低,适宜的温度.
解答:
解:(1)烟气脱硫、脱硝可以降低硫的氧化物、氮的氧化物含量,防止酸雨的发生,
故答案为:防止酸雨的发生;
(2))反应中氨气中的N元素由-3价升高为0价,化合价升高3价,泽尔转移3mol电子参加反应的氨气的物质的量为:
=1mol,根据方程式可知生成的氮气的物质的量为:1mol×
=
mol,
氮气的体积为:
mol×22.4L/mol=
L,
故答案为:
;
(3)①根据图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,反应总方程式为:6NO+3O2+2C2H4
3N2+4CO2+4H2O,
故答案为:6NO+3O2+2C2H4
3N2+4CO2+4H2O;
②由图可知,b曲线的最高点处,脱硝率高,负载率低,温度温度适宜,适宜适合条件为350℃、负载率3%,
故答案为:350℃、负载率3%.
故答案为:防止酸雨的发生;
(2))反应中氨气中的N元素由-3价升高为0价,化合价升高3价,泽尔转移3mol电子参加反应的氨气的物质的量为:
| 3mol |
| 3 |
| 3+2x |
| 4x |
| 3+2x |
| 4x |
氮气的体积为:
| 3+2x |
| 4x |
| 16.8+11.2x |
| x |
故答案为:
| 16.8+11.2x |
| x |
(3)①根据图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,反应总方程式为:6NO+3O2+2C2H4
| ||
故答案为:6NO+3O2+2C2H4
| ||
②由图可知,b曲线的最高点处,脱硝率高,负载率低,温度温度适宜,适宜适合条件为350℃、负载率3%,
故答案为:350℃、负载率3%.
点评:本题以烟气的脱硫和脱硝为载体,考查环境保护、氧化还原反应计算、方程式书写等知识,题目难度中等,本题注意把握数据处理和图象分析.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列事实中,能说明氯的非金属性比硫强的是( )
| A、次氯酸的氧化性比稀硫酸强 |
| B、氯化氢比硫化氢的热稳定性好 |
| C、高氯酸(HClO4)的酸性比硫酸强 |
| D、氯原子最外层电子数比硫原子的多 |
若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,肯定不能共存的是( )
| A、K+、NO3-、Cl-、Na+ |
| B、Ba2+、Mg2+、HCO3-、Cl- |
| C、NO3-、Na+、K+、CO32- |
| D、NO3-、K+、Cl-、OH- |
下列有关说法正确的是( )
| A、胶体能够较稳定存在的根本原因是胶粒作布朗运动 |
| B、铝丝和铜丝用导线连接后插入冷的浓硝酸溶液中构成原电池,铝为负极 |
| C、氯化钠投入到酒精中将形成胶体 |
| D、蛋白质溶液中加入氯化汞溶液能使其发生盐析 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol NaCl固体溶于1 L水所得溶液中NaCl的物质的量浓度为1 mol?L-1 |
| B、25℃,1.01×105Pa,64gSO2中含有的原子数为3NA |
| C、常温常压下,Zn和盐酸反应生成22.4L氢气时,Zn失去的电子数为2NA |
| D、标准状况下,11.2LH2O含有的分子数为0.5NA |