题目内容
甲、乙两车间排放出的污水中分别含有大量且不同的4种离子,这些离子是Ag+、Ba2+、Fe3+、Na+、Cl-、NO3-、OH-、SO42-.经检测,甲车间的污水pH>7,则下列判断正确的是( )
| A、甲车间的污水中可能含有Ba2+ |
| B、乙车间的污水中可能含有Na+ |
| C、甲车间的污水中不可能含有SO42- |
| D、乙车间的污水中一定含有Fe3+ |
考点:离子共存问题
专题:离子反应专题
分析:离子之间不能发生反应,即不能生成沉淀、气体、水.根据甲车间的污水pH>7,说明甲车间一定含有OH-,从而排除甲车间中一定没有Ag+、Fe3+;既然乙车间中含有Ag+、Fe3+,所以乙车间中不可能含有Cl-.结合均含4种离子来解答.
解答:
解:甲车间的污水pH>7,说明甲车间一定含有OH-,从而排除甲车间中一定没有Ag+、Fe3+,阳离子可能为Ba2+、Na+;
乙车间中含有Ag+、Fe3+,所以乙车间中不可能含有Cl-、SO42-,则阴离子为NO3-,共4种离子,则乙中含Ba2+,
综上所述,甲中含Na+、Cl-、OH-、SO42-,乙中含Ag+、Ba2+、Fe3+、NO3-,
故选D.
乙车间中含有Ag+、Fe3+,所以乙车间中不可能含有Cl-、SO42-,则阴离子为NO3-,共4种离子,则乙中含Ba2+,
综上所述,甲中含Na+、Cl-、OH-、SO42-,乙中含Ag+、Ba2+、Fe3+、NO3-,
故选D.
点评:本题考查离子的共存,为高频考点,把握pH及复分解反应的条件、各含4种离子为解答的关键,侧重分析与推断能力的考查,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知某温度下蒸馏水中的c(H+)=1×10-6mol/L,在此温度下将乙酸和氢氧化钠溶液混合,所得溶液的pH=7,此溶液中( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COO-)<c(Na+) |
| C、c(CH3C+OO-)=c(Na+) |
| D、无法确定c(CH3COO-)与c(Na+)的关系 |
下列说法错误的是( )
| A、书写热化学方程式时不但要注明反应物和生成物的状态,还需要注明反应环境的温度和压强 |
| B、HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为△H=2×(-57.3)kJ/mol |
| C、同一化学反应化学计量数不同,△H值不同,化学计量数相同而状态不同,△H值也不相同 |
| D、相同条件下,化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比 |
只用试管和胶头滴管无法区分的一组溶液是( )
| A、KOH和AlCl3 |
| B、AlCl3和氨水 |
| C、NaAlO2和盐酸 |
| D、Na2CO3和盐酸 |
化学与生产、生活密切相关,下列有关叙述正确的是( )
| A、晶体硅是“信息革命“的支柱材料,可用作光导纤维 |
| B、将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| C、化学反应伴随着能量的变化,反应物总能量一定大于生成物总能量 |
| D、含有碳的铜与稀H2SO4长时间接触会发生吸氧腐蚀 |
下列说法中,正确的是( )
| A、胆矾、漂白粉、氯化钾、石墨四种物质分别是按纯净物、混合物、电解质和非电解质的类别顺序排列的 |
| B、强电解质均是离子化合物 |
| C、碱性氧化物一定是金属氧化物 |
| D、酸性氧化物一定是非金属氧化物 |
新药“芬必得”主要成分的结构简式为: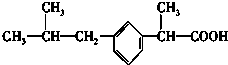 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、能发生酯化反应 |
| B、乙酸的同系物 |
| C、芳香烃 |
| D、含有两种官能团 |
利用下列实验装置能完成相应实验的是( )
A、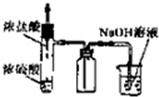 制取并吸收HCl |
B、 实验室制氨气 |
C、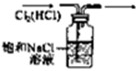 除去Cl2中的HCl |
D、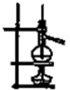 分离液体混合物 |
下列有关实验原理、方法和结论都正确的是( )
| A、用pH试纸测量溶液的pH值时要先将试纸润湿 |
| B、滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口如果试纸不变蓝说明原溶液中无NH4+ |
| C、取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| D、除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |