题目内容
13.处于相邻两个周期的主族元素A、B、C、D,它们原子半径依次减小.A离子和B离子的电子层相差2层,且能形成BA2型的离子化合物.C的离子带3个单位正电荷.D的气态氢化物通式为H2D,在其最高价氧化物中D质量分数为40%.D的原子序数大致等于其相对原子质量数值的一半.试回答:(1)A是Br,B是Mg,C是Al,D是S.
(2)B、C、D单质的还原性从大到小的顺序是Mg>Al>S.
(3)向D的氢化物的水溶液中滴入少量A单质,写出反应的化学方程式H2S+Br2═S↓+2HBr.
分析 处于相邻两个周期的主族元素A、B、C、D,它们原子半径依次减小.A离子和B离子的电子层相差2层,且能形成BA2型的离子化合物,B为+2价金属元素,A为-1价非金属元素,只有A为Br,B为Mg;C的离子带3个单位正电荷,C应为Al.D的气态氢化物通式为H2D,结合原子半径可知D为O或S,在其最高价氧化物中D质量分数为40%,D的原子序数大致等于其相对原子质量数值的一半,则D只能为S,原子序数为16,相对原子质量为32,三氧化硫中S的质量分数为40%符合题意,以此来解答.
解答 解:处于相邻两个周期的主族元素A、B、C、D,它们原子半径依次减小.A离子和B离子的电子层相差2层,且能形成BA2型的离子化合物,B为+2价金属元素,A为-1价非金属元素,只有A为Br,B为Mg;C的离子带3个单位正电荷,C应为Al.D的气态氢化物通式为H2D,结合原子半径可知D为O或S,在其最高价氧化物中D质量分数为40%,D的原子序数大致等于其相对原子质量数值的一半,则D只能为S,原子序数为16,相对原子质量为32,三氧化硫中S的质量分数为40%符合题意,
(1)由上述分析可知,A、B、C、D分别为Br、Mg、Al、S,故答案为:Br;Mg;Al;S;
(2)同周期,从左向右金属性减弱,则B、C、D单质的还原性从大到小的顺序是Mg>Al>S,故答案为:Mg>Al>S;
(3)向D的氢化物的水溶液中滴入少量A单质,该反应的化学方程式H2S+Br2═S↓+2HBr,故答案为:H2S+Br2═S↓+2HBr.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子结构及周期律推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.

 名校课堂系列答案
名校课堂系列答案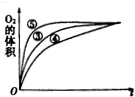 某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 分 组 实 验 | 催化剂 | |
| ① | 10mL 5%的H2O2溶液 | 无 |
| ② | 10mL 2%的H2O2溶液 | 无 |
| ③ | 10mL 5%的H2O2溶液 | 1mL 0.1mol/L的FeCl3溶液 |
| ④ | 10mL 5%的H2O2溶液+少量盐酸 | 1mL 0.1mol/L的FeCl3溶液 |
| ⑤ | 10mL 5%的H2O2溶液+少量NaOH溶液 | 1mL 0.1mol/L的FeCl3溶液 |
A.使反应活化能降低 B.使反应焓变减小 C.使平衡常数增大 D.使反应速率加快
(2)实验①和②的目的是探究反应物浓度对反应速率的影响.实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是:向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中).
(3)实验③④⑤中,测得生成O2的体积随时间变化关系如图.分析该图可得出的结论是:碱性环境可加快反应速率;酸性环境可减慢反应速率.
①HCl ②H2O ③N2 ④H2O2 ⑤CO2 ⑥C2H2.
| A. | ①②③ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
| A. | 10℃20mL 3mol/L的X溶液 | B. | 20℃30mL 2mol/L的X溶液 | ||
| C. | 20℃10mL 4mol/L的X溶液 | D. | 10℃10mL 2mol/L的X溶液 |

| A. | 加成反应 | B. | 消去反应 | C. | 取代反应 | D. | 还原反应 |
| 物质 | H2 | CO | CH4 |
| 燃烧热(kJ•mol-1) | 285.8 | 283.0 | 890.0 |
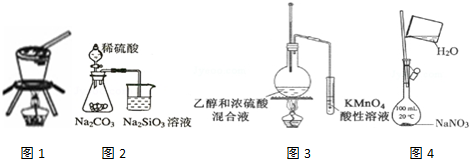
| A. | 用图1装置从饱和食盐水中提取NaCl晶体 | |
| B. | 用图2装置证明非金属性强弱 S>C>Si | |
| C. | 用图3装置验证乙烯的生成 | |
| D. | 用图4装置配制一定物质的量浓度的NaNO3溶液 |
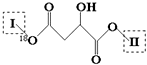 (其中I、II为未知部分的结构):为推测X的分子结构,现进行如图所示的转化.
(其中I、II为未知部分的结构):为推测X的分子结构,现进行如图所示的转化.
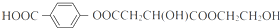 .
. .
.
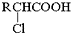 ;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH
;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH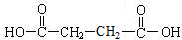 .
.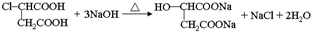 .
.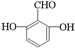 、
、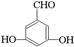 、
、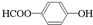 .
.