题目内容
 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子.下列有关说法正确的是( )
如图为冰晶体的结构模型,大球代表O原子,小球代表H原子.下列有关说法正确的是( )| A、冰晶体中每个水分子与另外四个水分子形成四面体 |
| B、冰晶体具有空间网状结构,是原子晶体 |
| C、水分子间通过H-O键形成冰晶体 |
| D、冰晶体熔化时,水分子之间的空隙增大 |
考点:晶胞的计算
专题:化学键与晶体结构
分析:在冰晶体中分子之间是通过氢键作用,是分子晶体,在每个水分子中氧原子按sp3方式杂化,每个水分子都可以与另外四个水分子形成氢键,而氢键具有方向性和饱和性,据此答题;
解答:
解:在冰晶体中分子之间是通过氢键作用,是分子晶体,在每个水分子中氧原子按sp3方式杂化,每个水分子都可以与另外四个水分子形成氢键,而氢键具有方向性和饱和性,
A、水分子中氧原子按sp3方式杂化,每个水分子都可以与另外四个水分子形成氢键,而氢键具有方向性,所以每个水分子与另外四个水分子形成四面体,故A正确;B、冰晶体虽然具有空间网状结构,但分子之间是氢键,所以是分子晶体,故B错误;
C、水分子之间是通过氢键作用的,故C错误;
D、由于氢键有方向性,分子之间的空隙较大,当晶体熔化时,氢键被破坏,水分子之间的空隙减小,故D错误;
故选A.
A、水分子中氧原子按sp3方式杂化,每个水分子都可以与另外四个水分子形成氢键,而氢键具有方向性,所以每个水分子与另外四个水分子形成四面体,故A正确;B、冰晶体虽然具有空间网状结构,但分子之间是氢键,所以是分子晶体,故B错误;
C、水分子之间是通过氢键作用的,故C错误;
D、由于氢键有方向性,分子之间的空隙较大,当晶体熔化时,氢键被破坏,水分子之间的空隙减小,故D错误;
故选A.
点评:本题主要考查了氢键的相关知识,较容易,解题关键是对基础知识的掌握.

练习册系列答案
相关题目
在一个绝热的体积一定的密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g);△H<0下列各项中不能说明该反应已经达到平衡状态的是( )
| A、体系的压强不再改变 |
| B、体系的温度不再改变 |
| C、断裂1mol N≡N键的同时,也断裂6molN-H键 |
| D、反应消耗的N2、H2与产生的NH3的速率υ(N2):υ(H2):υ(NH3)=1:3:2 |
分别将0.2mol的Na、Mg、Al投入500mL浓度为为0.2mol/L的盐酸中,生成氢气的质量比为( )
| A、1:2:3 |
| B、.1:1:1 |
| C、3:2:1 |
| D、2:1:1 |
由沸点数据:甲烷-161.7℃、乙烷-88.6℃、丁烷-0.5℃、戊烷 36.1℃,可判断丙烷的沸点可能是( )
| A、高于-0.5℃ |
| B、约是 30℃ |
| C、约是-40℃ |
| D、低于-88.6℃ |
下列有关化学概念逻辑关系正确的是( )
A、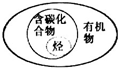 |
B、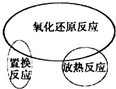 |
C、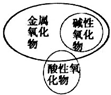 |
D、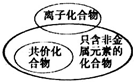 |
下列各图若为元素周期表的一部分(表中数字为原子序数),其中正确的是( )
A、 |
B、 |
C、 |
D、 |
下列物质中的n相等时,其同类别的同分异构体数目最多的是( )
| A、烃CnH2n+2 |
| B、醇CnH2n+2O |
| C、醛CnH2nO |
| D、羧酸CnH2nO2 |
某一元有机酸HA的溶液中,若未电离的HA分子个数与溶液中的离子个数比为a:b,则HA的电离度(即转化率)是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
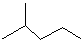 表示的分子式
表示的分子式 中含有的官能团的名称为
中含有的官能团的名称为