题目内容
下列事实能说明醋酸属于弱电解质的是( )
①中和10ml1mol/LCH3COOH溶液需要10ml1mol/LNaOH溶液
②物质的量溶液相同时,锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01mol/L醋酸溶液pH的大于2
④0.1mol/LCH3COONa溶液显碱性.
①中和10ml1mol/LCH3COOH溶液需要10ml1mol/LNaOH溶液
②物质的量溶液相同时,锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01mol/L醋酸溶液pH的大于2
④0.1mol/LCH3COONa溶液显碱性.
| A、①②③ | B、②③④ |
| C、①③④ | D、①④ |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:证明醋酸是弱电解质,可证明存在电离平衡、部分电离或对应的强碱盐溶液呈碱性,以此解答.
解答:
解:①酸碱的物质的量相同,完全发生中和反应,与酸的强弱无关,不能证明为弱酸,故错误;
②开始时锌粒跟盐酸反应的速率比跟醋酸反应的速率快,说明等浓度的盐酸溶液中氢离子浓度大,则可说明醋酸为弱酸,故正确;
③0.01mol/L醋酸溶液的pH=3,说明醋酸没有完全电离,可证明为弱酸,故正确;
④CH3COONa溶液显碱性,可说明为强碱弱酸盐,可证明醋酸为弱酸,故正确.
故选B.
②开始时锌粒跟盐酸反应的速率比跟醋酸反应的速率快,说明等浓度的盐酸溶液中氢离子浓度大,则可说明醋酸为弱酸,故正确;
③0.01mol/L醋酸溶液的pH=3,说明醋酸没有完全电离,可证明为弱酸,故正确;
④CH3COONa溶液显碱性,可说明为强碱弱酸盐,可证明醋酸为弱酸,故正确.
故选B.
点评:本题考查弱电解质的判断,明确弱电解质的性质是解答本题的关键,常用的方法是利用电离的不完全性.

练习册系列答案
相关题目
用标准的NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作会导致实验结果偏低的是( )
| A、碱式滴定管用蒸馏水洗净后没有用标准液润洗 |
| B、锥形瓶用蒸馏水洗净后没用待测液润洗 |
| C、滴定管尖端气泡没有排除,滴定后消失 |
| D、终点读数时俯视 |
下列关于物质用途的叙述中,不正确的是( )
| A、硅可以用做制造变压器铁芯的材料 |
| B、二氧化硅可用于制造光导纤维 |
| C、水玻璃可以用作木材防火剂 |
| D、石墨可用作绝缘材料 |
在523K时,有以下反应:2HCl(g)+CrO3(g)═CrO2Cl2(g)+H2O(g)+Q (Q>0),反应进行至第5min时,改变某个条件,当反应进行至第10min时,发现生成CrO2Cl2(g)的速率增大,CrO2Cl2的百分含量也增大,则改变的条件不可能是( )
| A、加热 | B、使用催化剂 |
| C、加压 | D、分离出水气 |
钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为W(s)+2I2(g)
WI4(g).下列说法正确的是( )
| 1400℃ |
| 约3000℃ |
| A、温度越高,灯丝的使用寿命越长 |
| B、WI4在灯丝上分解,产生的W又沉积在灯丝上 |
| C、WI4在灯管壁上分解,使灯管的寿命延长 |
| D、温度升高时,WI4的分解速率加快,W和I2的化合速率减慢 |
关于如图所示的原电池,下列说法正确的是 ( )
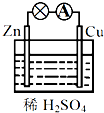

| A、锌棒为正极 |
| B、铜棒上发生还原反应 |
| C、正极反应为Cu-2e-=Cu2+ |
| D、电流从锌棒经外电路流向铜棒 |
基因测序研究中,常用
P作标记物,下列关于
P的说法正确的是( )
32 15 |
32 15 |
| A、质子数为32 |
| B、质量数为15 |
| C、32P与33P互为同位素 |
| D、中子数为15 |