题目内容
10.①纯碱;②火碱;③氯水;④小苏打.(1)以上物质中属于混合物的是③;属于碱的是②;具有漂白性的是③;既能与盐酸反应,又能与氢氧化钠反应的是④.(填序号)
(2)纯碱在水中的电离方程式为Na2CO3=2Na++CO32-.
(3)小苏打与稀盐酸反应的离子方程式为H++HCO3-=CO2↑+H2O.
分析 (1)不同物质组成的为混合物,水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱,二氧化硫具有漂白性,既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的铵盐(如(NH4)2CO3等)、弱酸的酸式盐(NaHCO3、NaHS等)、单质(如Al)、氨基酸等;
(2)Na2CO3在溶液中完全电离出钠离子和碳酸根离子;
(3)小苏打与稀盐酸反应生成氯化钠、二氧化碳和水.
解答 解:(1)①纯碱是碳酸钠属于盐为纯净物,与盐酸反应,与氢氧化钠溶液不反应;
②火碱是氢氧化钠,属于纯净物,水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱;
③氯水属于混合物,氯水中的HClO具有强氧化性,具有漂白性;
④小苏打是碳酸氢钠属于纯净物,能与盐酸和氢氧化钠溶液反应;
属于混合物的是③,属于碱的是②,具体有漂白性的是③,既能与盐酸反应,又能与氢氧化钠反应的是④,
故答案为:③;②;③;④;
(2)Na2CO3在溶液中完全电离出钠离子和碳酸根离子,其电离方程式为:Na2CO3=2Na++CO32-;
故答案为:Na2CO3=2Na++CO32-;
(3)小苏打与稀盐酸反应生成氯化钠、二氧化碳和水,其反应的离子方程式为:H++HCO3-=CO2↑+H2O;
故答案为:H++HCO3-=CO2↑+H2O.
点评 本题考查了物质分类、物质性质、电解质电离、离子方程式等知识点,掌握基础是解题关键,题目难度不大,注意把握酸、碱、盐、混合物等概念以及离子方程式的书写方法.

练习册系列答案
相关题目
18.下列逻辑关系图中正确的是( )
| A. | 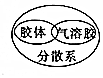 | B. | 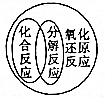 | C. | 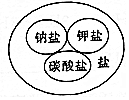 | D. | 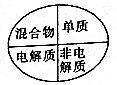 |
5.实验室可以用来直接加热的玻璃仪器是( )
| A. | 小试管 | B. | 容量瓶 | C. | 量筒 | D. | 蒸发皿 |
15.下列水解反应离子方程式书写正确的是( )
| A. | CH3COOH+OH-?CH3COO-+H2O | B. | S2-+2H2O?H2S+2OH- | ||
| C. | CH3COOH+H2O?CH3COO-+H3O+ | D. | CO32-+H2O?HCO3-+OH- |
2.《中国能源矿产地质调查报告》显示我国天然气水合物超千亿吨油当量.天然气主要成分为( )
| A. | H2 | B. | CO | C. | CH4 | D. | C2H4 |
19.用蘸有浓氨水的棉棒检漏输氯管道的原理为:3Cl2+8NH3═N2+6NH4Cl.该反应的下列说法正确的是( )
| A. | 35.5g氯气所含的分子数为6.02×1023 | |
| B. | 常温常压下,22.4L氨气所含原子总数为4×6.02×1023 | |
| C. | 反应每生成1molN2转移电子数约为6×6.02×1023 | |
| D. | 1mol•L-1NH4Cl溶液中,含有Cl-数约为6.02×1023 |