题目内容
18.下列说法中正确的是( )| A. | 所有物质中都存在化学键 | |
| B. | 由两种元素组成的分子中一定不存在非极性共价键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 化学键断裂的过程必发生化学反应 |
分析 A、稀有气体分子中不存化学键;
B、两种元素组成的分子中可能含有非极性键;
C、含有离子键的化合物是离子化合物;
D、电解质溶于水中发生化学键断裂.
解答 解:A、稀有气体分子中不存化学键,故A错误;
B、两种元素组成的分子中可能含有非极性键,如乙烯、双氧水、肼等,故B错误;
C、含有离子键的化合物一定是离子化合物,故C正确;
D、电解质溶于水中发生化学键断裂,如氯化钠溶于水离子键断裂,但是物理变化,故D错误;
故选C.
点评 本题考查物质中存在的化学键,明确物质的构成微粒及微粒之间作用力即可解答,会采用举例法解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.砹(At)与F、Cl、Br、I同主族,推测砹AA或砹的化合物不可能具有的性质是( )
| A. | 砹单质是有色固体 | |
| B. | 非金属性:At>I | |
| C. | HAt的稳定性比HI的弱 | |
| D. | I2可以从At的可溶性盐溶液中置换出来At2 |
3.下列说法正确的是( )
| A. | CS2分子中σ键与π键的数目之比是2:1 | |
| B. | 分子中含有非极性键,该分子一定是非极性分子 | |
| C. | NaOH是含有非极性共价键的离子化合物 | |
| D. | 在元素周期表中,d区和ds区的元素都是金属元素 |
10.同周期的X、Y、Z三元素,其最高价氧化物水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则下列判断正确的是( )
| A. | 原子半径 X>Y>Z | |
| B. | 非金属性 X>Y>Z | |
| C. | X、Y、Z的单质与氢气化合能力由弱到强 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
7.下列化合物不能用相应元素的单质直接化合而成的是( )
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦FeCl3.
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦FeCl3.
| A. | ②⑤ | B. | ①④⑥ | C. | ③④ | D. | ④⑥⑦ |
8.下列数值都是烃的相对分子质量,其对应的烃一定为烷烃的是( )
| A. | 54 | B. | 128 | C. | 42 | D. | 58 |
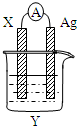 依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.
依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.