题目内容
8.如图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请回答下列问题:
(1)写出铜和稀硝酸反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)与装置甲相比,装置乙的优点是①可观察NO的生成及NO被氧化 ②操作现象明显
(3)若用实验装置甲进行实验,能否证明铜和稀硝酸反应的产物是NO气体:不能,圆底烧瓶内含有空气,NO与氧气反应,生成红棕色NO2,若产生的是NO2,NO2与水反应产生NO
(4)若用实验装置乙进行实验,实验前如何检验装置乙的气密性闭活塞b打开活塞a,通过分液漏斗向U型管内加水至左边液面高于右边,若能保持此状态一段时间,则说明该装置的气密性良好.
分析 (1)铜和稀硝酸反应生成硝酸铜、一氧化氮、水.
(2)实验装置甲烧瓶内有空气,不易观察NO的生成,且操作现象明显;
(3)NO与空气中的氧气反应生成红棕色的二氧化氮;
(4)利用干燥管内外形成液面高度差检验装置气密性,根据液面的高度的变化判断气密性.
解答 解:(1)铜和稀硝酸反应生成硝酸铜、一氧化氮、水,反应离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(2)实验装置甲烧瓶内有空气,NO与空气中的氧气反应生成红棕色的二氧化氮,反应方程式为2NO+O2═2NO2,而乙中开始U型管中充满硝酸,没有空气,可观察NO的生成及NO被氧化,操作现象明显,
故答案为:可观察NO的生成及NO被氧化;操作现象明显;
(3)二氧化氮与水反应生成一氧化氮,所以甲虽然收集到的气体是NO,但并不能说明反应中一定生成NO,也有可能生成二氧化氮,因为甲是用排水法收集气体的,圆底烧瓶内含有空气,NO与氧气反应,生成红棕色NO2,不能证明铜和稀硝酸反应的产物是NO气体.
故答案为:不能,圆底烧瓶内含有空气,NO与氧气反应,生成红棕色NO2,若产生的是NO2,NO2与水反应产生NO;
(4)利用干燥管内外形成液面高度差检验装置气密性,操作为关闭活塞b打开活塞a,通过分液漏斗向U型管内加水至左边液面高于右边,若能保持此状态一段时间,则说明该装置的气密性良好,
故答案为:关闭活塞b打开活塞a,通过分液漏斗向U型管内加水至左边液面高于右边,若能保持此状态一段时间,则说明该装置的气密性良好.
点评 本题考查性质实验方案的设计,为高频考点,把握实验装置的作用、物质的性质、发生的反应及实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| A. | 甲、乙提高相同温度 | B. | 甲中加入1molHe,乙不变 | ||
| C. | 甲降低温度,乙不变 | D. | 甲增加1molH2,乙增加1molI2 |
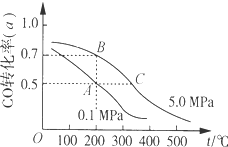
| A. | A、B两点表示在某时刻达到平衡状态,此时A、B两点时容器中,n(A)总:n(B)总=4:5 | |
| B. | 在A点时保持恒温恒容,再向体系中充入少量He,重新达到平衡前v(正)>v(逆) | |
| C. | 若开始时向容器中充入1mol CO与2mol H2,达到平衡(与A点相同温度压强)时,CO的 转化率小于50% | |
| D. | 在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率 |
①18g D2O含有的电子数为10NA
②同温、同压下,相同体积的氟气和氩气所含的原子数相等
③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
④在标准状况下,22.4LSO3的物质的量为1mol
⑤4℃时5.4mL的水所含的原子总数为0.9NA
⑥1mol Na2O2与水完全反应时转移电子数为2NA.
| A. | ①②④⑥ | B. | ①②③⑤ | C. | ①③⑤⑥ | D. | ③④⑤⑥ |
| A. | H2SO4?2H++SO42- | B. | BaCl2═Ba2++2Cl- | ||
| C. | NH3•H2O═NH4++OH- | D. | Na2CO3═Na++CO32- |
| A. | 化合反应一定是氧化还原反应 | B. | 非金属氧化物一定是酸性氧化物 | ||
| C. | 金属氧化物一定是碱性氧化物 | D. | 碱性氧化物一定是金属氧化物 |
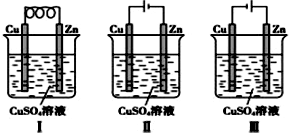
| A. | Ⅰ是原电池,Ⅱ是电镀装置 | |
| B. | Ⅰ、Ⅱ装置中锌极上均发生氧化反应 | |
| C. | Ⅱ、Ⅲ装置中,铜极均发生氧化反应而溶解 | |
| D. | Ⅱ、Ⅲ装置中Cu2+浓度基本不变 |
| A. | 放电时,Mo3S4发生氧化反应 | |
| B. | 放电时,负极反应式:Mo3S4+2xe-→Mo3S42x- | |
| C. | 充电时,Mg2+向阴极迁移 | |
| D. | 充电时,阳极反应式:xMg2++2xe-→xMg |