题目内容
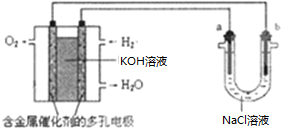
某实验小组利用H2(g)、O2(g)、KOH(aq)设计成电池装置.
(1)请写出该氢氧燃料电池的负极的电极反应式为 ;
(2)若用该燃料电池电解500mL饱和食盐水,已知a、b两极为惰性电极,b电极的电极反应式为 .请写出电解池总的离子方程式为 .电解一段时间后,a电极共集到气体560ml(折算成标准状况下),则所得溶液的pH= (不考虑气体的溶解及电解前后溶液体积的变化.NaCl没有完全反应)
(1)请写出该氢氧燃料电池的负极的电极反应式为
(2)若用该燃料电池电解500mL饱和食盐水,已知a、b两极为惰性电极,b电极的电极反应式为

考点:电解原理,原电池和电解池的工作原理
专题:
分析:(1)用H2(g)、O2(g)、KOH(aq)形成原电池,负极通入氢气,发生氧化反应;正极通入氧气,发生还原反应;
(2)电解饱和食盐水阳极是氯离子失电子生成氯气,阴极是氢离子得到电子生成氢气;依据电解原理分析,书写电池反应,依据生成的气体体积.计算氢氧根离子浓度,结合离子积常数计算氢离子浓度计算溶液pH.
(2)电解饱和食盐水阳极是氯离子失电子生成氯气,阴极是氢离子得到电子生成氢气;依据电解原理分析,书写电池反应,依据生成的气体体积.计算氢氧根离子浓度,结合离子积常数计算氢离子浓度计算溶液pH.
解答:
解:(1)用H2(g)、O2(g)、KOH(aq)形成原电池,负极通入氢气,发生氧化反应,电极反应式为:H2+2e-+2OH-=2H2O;
故答案为:H2+2e-+2OH-=2H2O;
(2)b电极与原电池的正极相连,为电解池的阳极,阳极上发生氧化反应,氯离子失电子生成氯气,电极反应式为:2Cl--2e-=Cl2↑;
电解饱和食盐水生成氢氧化钠、氯气和氢气,离子方程式为:2Cl-+2H2O=H2↑+Cl2↑2+2OH-;
a电极氢离子得到电子生成氢气,生成氢气560ml的物质的量=
=0.025mol,依据电解方程式:
2Cl-+2H2O=H2↑+Cl2↑2+2OH-;
1 2
0.025mol n
=
解得:n=0.05mol
C(OH-)=
=0.1mol/L,
C(H+)=
=10-13mol/L,pH=-lg[H+]=13;
故答案为:2Cl--2e-=Cl2↑;2Cl-+2H2O=H2↑+Cl2↑2+2OH-;13;
故答案为:H2+2e-+2OH-=2H2O;
(2)b电极与原电池的正极相连,为电解池的阳极,阳极上发生氧化反应,氯离子失电子生成氯气,电极反应式为:2Cl--2e-=Cl2↑;
电解饱和食盐水生成氢氧化钠、氯气和氢气,离子方程式为:2Cl-+2H2O=H2↑+Cl2↑2+2OH-;
a电极氢离子得到电子生成氢气,生成氢气560ml的物质的量=
| 0.56L |
| 22.4L/mol |
2Cl-+2H2O=H2↑+Cl2↑2+2OH-;
1 2
0.025mol n
| 1 |
| 0.025mol |
| 2 |
| n |
C(OH-)=
| 0.05mol |
| 0.5L |
C(H+)=
| Kw |
| C(OH-) |
| 10-14 |
| 0.1 |
故答案为:2Cl--2e-=Cl2↑;2Cl-+2H2O=H2↑+Cl2↑2+2OH-;13;
点评:本题考查原电池、电解池工作原理,正确推断燃料电池正负极是解本题的关键,难点是溶液的pH计算,根据电解饱和食盐水的离子方程式分析解答.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
下列离子方程式正确的是( )
| A、碳酸钙和硝酸反应:CO32-+2H+═H2O+CO2↑ |
| B、向KOH溶液中加盐酸:H++OH-═H2O |
| C、铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-═BaSO4↓ |
下列各电离方程式中,书写正确的是( )
| A、CH3COOH?H++CH3COO- |
| B、KHSO4?K++H++SO42- |
| C、Al(OH)3?Al3++3OH- |
| D、NaH2PO4?Na++H2PO42- |
胶体和溶液的根本区别在于( )
| A、外观是否均一 |
| B、分散质粒子是否带电荷 |
| C、分散质粒子的大小 |
| D、分散系是否有颜色 |
下列按混合物、纯净物、电解质和非电解质顺序排列的是( )
| A、盐酸、空气、醋酸、干冰 |
| B、漂白粉、胆矾、氯化钾、硫酸钡 |
| C、蛋白质、油脂、苛性钾、碳酸钙 |
| D、福尔马林、冰醋酸、硫酸钠、乙醇 |
将下列各物质分别按等物质的量混合后加水溶解,有沉淀生成的是( )
| A、Na2CO3,NaAlO2,NaOH |
| B、AlCl3,K2SO4,HCl |
| C、CaCl2,Na2CO3,NaOH |
| D、AlCl3,Ba(OH)2,HNO3 |
有M、N两种溶液,各含有下列12种离子中的6种,且所含离子各不相同:Al3+、Na+、K+、Cl-、NO3-、OH-、Fe3+、Ba2+、H+、SO32-、MnO4-、AlO2-.已知每组溶液中的阳离子至少有2种,则下列说法正确的是( )
| A、若溶液M呈强酸性,则N中一定含有OH-、NO3- |
| B、若溶液N呈强酸性,则N中一定含有Al3+、可能含有Na+ |
| C、若溶液N无色,则N中一定不含有Fe3+、Cl-,且溶液M有强氧化性 |
| D、常温下,若M、N两溶液混合后pH=7,则至少生成三种沉淀 |
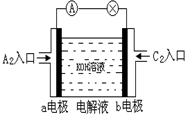 现有A、B、C、D、E五种短周期元素,已知:①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;②A、D同主族,A是所有元素中原子半径最小的元素;③通常状况下,A2、B2、C2三种单质均为常见无色气体;④B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素.请填写下列空白:
现有A、B、C、D、E五种短周期元素,已知:①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;②A、D同主族,A是所有元素中原子半径最小的元素;③通常状况下,A2、B2、C2三种单质均为常见无色气体;④B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素.请填写下列空白: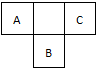 短周期元素的A、B、C,在元素周期表中的位置如图所示,已知A元素单质是空气中含量最多的气体,A、C两种元素的原子核外电子数之和等于B元素的质子数,据此填空:
短周期元素的A、B、C,在元素周期表中的位置如图所示,已知A元素单质是空气中含量最多的气体,A、C两种元素的原子核外电子数之和等于B元素的质子数,据此填空: