题目内容
4.反应2A(g)?2B(g)+E(g)△H>0,达到平衡时,要使正反应速率降低,且B的物质的量增大,应采取的措施是( )| A. | 加压 | B. | 增大体积 | C. | 减少A的浓度 | D. | 降温 |
分析 达平衡时,要使v正降低,可采取降低温度、减小压强或减小浓度的措施,且使B的物质的量增大,应使平衡向正反应方向移动,结合平衡移动原理分析解答.
解答 解:A.增大压强,平衡向逆反应方向移动,B的浓度减小,正、逆反应速率都增大,故A错误;
B.增大体积相当于减小体系的压强,正反应速率降低,正反应方向为体积增大的反应,平衡向正反应方向移动,B的物质的量增大,故B正确;
C.减少A的浓度,正反应速率降低,平衡向逆反应移动,B的物质的量减小,故C错误;
D.该反应正反应是吸热反应,降温,平衡向逆反应方向移动,B的物质的量减小,但正、逆反应速率都减小,故D错误;
故选B.
点评 本题考查外界条件对化学平衡的影响,难度不大,本题注意根据反应方程式的特征判断平衡移动的方向.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.检验制得的HCl气体中混有少量Cl2的方法是( )
| A. | 观察气体的颜色 | B. | 用干燥的蓝色石蕊试纸 | ||
| C. | 用硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
15.NA代表阿伏加德罗常数,下列叙述错误的是( )
| A. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| B. | 在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则消耗NA个Cl2分子 | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g | |
| D. | 一定温度下,1 L 0.50 mol•L-1 NaCl溶液与2 L 0.25 mol•L-1 Na2CO3溶液含Na+的物质的量不同 |
12.已知,298K时,下列反应的有关数据:
C(s)+$\frac{1}{2}$O2 (g)═CO(g)△H1=-110.5KJ/mol
C(s)+O2(g)═CO2(g)△H2=-393.5KJ/mol
则C(s)+CO2(g)═2CO (g)的△H为( )
C(s)+$\frac{1}{2}$O2 (g)═CO(g)△H1=-110.5KJ/mol
C(s)+O2(g)═CO2(g)△H2=-393.5KJ/mol
则C(s)+CO2(g)═2CO (g)的△H为( )
| A. | +172.5KJ/mol | B. | -172.5KJ/mol | C. | -110.5KJ/mol | D. | -504 KJ/mol |
19.工业制取C1O2的化学反应:2NaC1O3+SO2+H2SO4═2ClO2+2NaHSO4,下列说法正确的是( )
| A. | SO2在反应中被还原成NaHSO4 | |
| B. | NaC1O3在反应中失去电子 | |
| C. | H2SO4在反应中作氧化剂 | |
| D. | 若反应中转移1mol电于,则生成1mol C1O2 |
9.下列说法正确的是( )
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 结构简式为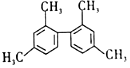 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 |
16.化学与生产、生活、社会密切相关.下列有关说法中,正确的是( )
| A. | 从海水中可以得到 NaCl,电解饱和 NaCl 溶液可制备 Na | |
| B. | 锅炉水垢中含有的 CaSO4,可先用 Na2CO3溶液处理,后用酸除去 | |
| C. | 网络飞速发展,得益于光纤良好的导电性,光纤的主要成分是高纯度的单质硅 | |
| D. | 钢铁器件镀金既能增加美观,又能在镀层局部破损后防止器件损耗 |
8.下列反应的离子方程式正确的是( )
| A. | NaHCO3溶液与盐酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 硝酸银溶液与铜:Cu+Ag+═Cu2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++CO32- | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+H2O+CO2↑ |
9.下列各组物质中,含分子数最多的是( )
| A. | 0.4 mol NH3 | B. | 6.02×1023个硫酸分子 | ||
| C. | 10g氖气 | D. | 4℃时54 mL水 |