题目内容
16.下列离子可以大量共存的是( )| A. | Mg2+ Na+ SO42- OH- | B. | Ca2+K+ HCO3-OH- | ||
| C. | Na+ H+ CH3COO- SO42- | D. | Ba2+ K+NO3-Cl- |
分析 根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,以此来解答.
解答 解:A.Mg2+、OH-结合生成沉淀,不能共存,故A错误;
B.Ca2+、HCO3-、OH-结合生成沉淀和水,不能共存,故B错误;
C.H+、CH3COO-结合生成弱酸,不能共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
6.关于水的离子积常数,下列说法中不正确的是( )
| A. | 纯水中c(H+)•c(OH-)=1×10-14 | B. | 25℃纯水中c(H+)•c(OH-)=1×10-14 | ||
| C. | 25℃稀盐酸中c(H+)•c(OH-)=1×10-14 | D. | KW值随温度升高而增大 |
7.下列叙述中正确的是(NA为阿伏加德罗常数)( )
| A. | 1mol Na与足量水反应,转移电子数为NA | |
| B. | 同温同压下,相同体积的物质,其物质的量必相等 | |
| C. | 5.3g Na2CO3固体含有的离子数为1.5NA | |
| D. | 标准状况下,22.4L H2O所含的原子数为3 NA |
4.下列物质只含有离子键的是( )
| A. | H2O | B. | CO2 | C. | Na2O | D. | NH4Cl |
11.关于如图所示装置的叙述,不正确的是( )
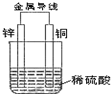

| A. | 铜片上有气泡产生 | B. | 铜片质量逐渐减少 | ||
| C. | 电子从锌片经导线流向铜 | D. | 该装置把化学能转化为电能 |
1.锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性.下列关于锂的判断可能正确的是( )
| A. | Li能在空气中燃烧 | B. | Li2O只有共价键 | ||
| C. | Li2CO3能溶于水 | D. | LiOH受热不分解 |
5.反应N2(g)+3H2(g)?2NH3(g)△H<0;若升温,则反应速率v(正)、v(逆)的变化是( )
| A. | 同时减少 | B. | 同时增大 | C. | v(正)增大,v(逆)减少 | D. | v(正)减少,v(逆)增大 |
6.W、X、Y、Z是原子序数依次增大的四种短周期主族元素,W原子在周期表中原子半径最小,X与Y原子最外层电子数之和为8,X的最高正价与最低负价代数和为2,Z原子的最外层电子数是Y原子最外层电子数的2倍,下列说法正确的是( )
| A. | 单质沸点:X>Y | B. | 阳离子的氧化性:W>Y | ||
| C. | 氧化物的水化物的酸性:Z>X | D. | Y、Z的简单离子均能抑制水的电离 |