题目内容
根据下表提供的数据,判断下列离子方程式或化学方程式正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K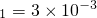 |
K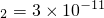 |
- A.向Na2CO3溶液中滴加少量氯水:CO
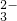 +2Cl2+H2O=2Cl-+2HClO+CO2
+2Cl2+H2O=2Cl-+2HClO+CO2 - B.向NaHCO3溶液中滴加少量氯水:2HCO
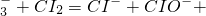 2CO2+H2O
2CO2+H2O - C.向NaClO溶液中通入少量CO2:CO2+NaClO+H2O=NaHCO3+HClO
- D.向NaClO溶液通入足量CO2:CO2+2NaClO+H2O=Na2CO3+2HClO
C
分析:依据电离常数分析可知酸性为H2CO3>HClO>HCO3-,依据酸性强弱分析可能发生的反应产物;
A、碳酸钠溶液中滴入氯水,次氯酸和碳酸钠反应生成碳酸氢钠和次氯酸钠;
B、向NaHCO3溶液中滴加少量氯水,氯水中的元素和碳酸氢钠反应生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物为次氯酸;
C、向NaClO溶液中通入少量CO2反应生成碳酸氢钠和次氯酸;
D、向NaClO溶液通入足量CO2,反应生成碳酸氢钠和次氯酸.
解答:依据电离常数分析可知酸性为H2CO3>HClO>HCO3-,酸性强的可以反应得到酸性弱的,据此分析判断;
A、向Na2CO3溶液中滴加少量氯水,溶液中碳酸钠过量,盐酸和碳酸钠反应生成碳酸氢钠,次氯酸和碳酸钠反应生成碳酸氢钠和次氯酸钠,反应的离子方程式应为:2CO32-+2Cl2+H2O=2Cl-+ClO-+2HCO3-,故A错误;
B、向NaHCO3溶液中滴加少量氯水,氯水中的元素和碳酸氢钠反应生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物为次氯酸,反应的离子方程式为:
HCO3-+Cl2=Cl-+HClO+CO2↑,故B错误;
C、向NaClO溶液中通入少量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故C正确;
D、向NaClO溶液中通入足量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故D错误;
故选C.
点评:本题考查了弱电解质电离平衡常数的分析判断,主要是与碳酸钠反应的产物分析判断是解题关键,题目难度中等.
分析:依据电离常数分析可知酸性为H2CO3>HClO>HCO3-,依据酸性强弱分析可能发生的反应产物;
A、碳酸钠溶液中滴入氯水,次氯酸和碳酸钠反应生成碳酸氢钠和次氯酸钠;
B、向NaHCO3溶液中滴加少量氯水,氯水中的元素和碳酸氢钠反应生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物为次氯酸;
C、向NaClO溶液中通入少量CO2反应生成碳酸氢钠和次氯酸;
D、向NaClO溶液通入足量CO2,反应生成碳酸氢钠和次氯酸.
解答:依据电离常数分析可知酸性为H2CO3>HClO>HCO3-,酸性强的可以反应得到酸性弱的,据此分析判断;
A、向Na2CO3溶液中滴加少量氯水,溶液中碳酸钠过量,盐酸和碳酸钠反应生成碳酸氢钠,次氯酸和碳酸钠反应生成碳酸氢钠和次氯酸钠,反应的离子方程式应为:2CO32-+2Cl2+H2O=2Cl-+ClO-+2HCO3-,故A错误;
B、向NaHCO3溶液中滴加少量氯水,氯水中的元素和碳酸氢钠反应生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物为次氯酸,反应的离子方程式为:
HCO3-+Cl2=Cl-+HClO+CO2↑,故B错误;
C、向NaClO溶液中通入少量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故C正确;
D、向NaClO溶液中通入足量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故D错误;
故选C.
点评:本题考查了弱电解质电离平衡常数的分析判断,主要是与碳酸钠反应的产物分析判断是解题关键,题目难度中等.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
|
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
|
根据下表提供的数据,判断下列离子方程式或化学方程式正确的是( )
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=3×10-3 |
| K2=3×10-11 |
| A、向Na2CO3溶液中滴加少量氯水:CO32-+2Cl2+H2O=2Cl-+2HClO+CO2 |
| B、向NaHCO3溶液中滴加少量氯水:2HCO3-+CI2=CI-+CIO-+2CO2+H2O |
| C、向NaClO溶液中通入少量CO2:CO2+NaClO+H2O=NaHCO3+HClO |
| D、向NaClO溶液通入足量CO2:CO2+2NaClO+H2O=Na2CO3+2HClO |
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
A.c(HCO3-)>c(ClO-)>c(OH-)
B.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+C(OH-)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
D.c(Na+)=c(HCO3-)+ c(CO32-) + c(H2CO3) +c(ClO-) +c(HClO)
 、
、 混合溶液中,各种离子浓度关系正确的是
混合溶液中,各种离子浓度关系正确的是

 B、
B、

