题目内容
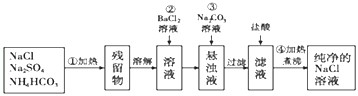
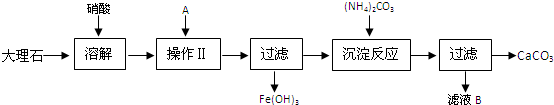
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示.(已知:碳酸不能溶解Al(OH)3沉淀)

(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
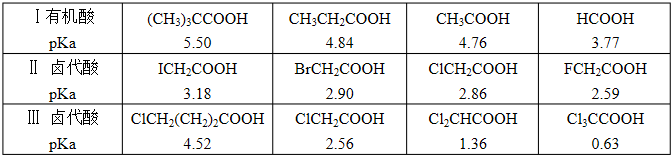
a.酸性:H2CO3>H2SiO3 b.结合质子的能力:CO
>AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4 d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是 通过 现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是 , ;若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1molL-1 HNO3的体积为 L.

(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3 b.结合质子的能力:CO
2- 3 |
c.稳定性:H2O>CH4>SiH4 d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是
考点:物质分离和提纯的方法和基本操作综合应用,硅和二氧化硅,镁、铝的重要化合物,铁的氧化物和氢氧化物
专题:实验设计题,元素及其化合物
分析:(1)滤渣中含有二氧化硅,高温下碳与二氧化硅反应生成硅和CO;
(2)a.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
b.酸性越弱,相应的酸根越容易结合氢离子;
c.元素的非金属性越强,对应的氢化物越稳定;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小;
(3)矿石加硝酸生成气体,可说明含有FeCO3,加入过量NaoH溶液后通入过量二氧化碳没有沉淀生成,说明没有Al2O3,滤渣溶解后加入盐酸生成胶状沉淀,说明含有SiO2;
(4)矿石含有FeCO3,可与HNO3反应生成铁离子、二氧化碳、一氧化氮气体,据此写出碳酸亚铁与稀硝酸反应的离子方程式;
(5)处理该矿石,逸出的气体为NO,可与氧气反应生成硝酸,可循环利用,结合反应的方程式计算.
(2)a.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
b.酸性越弱,相应的酸根越容易结合氢离子;
c.元素的非金属性越强,对应的氢化物越稳定;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小;
(3)矿石加硝酸生成气体,可说明含有FeCO3,加入过量NaoH溶液后通入过量二氧化碳没有沉淀生成,说明没有Al2O3,滤渣溶解后加入盐酸生成胶状沉淀,说明含有SiO2;
(4)矿石含有FeCO3,可与HNO3反应生成铁离子、二氧化碳、一氧化氮气体,据此写出碳酸亚铁与稀硝酸反应的离子方程式;
(5)处理该矿石,逸出的气体为NO,可与氧气反应生成硝酸,可循环利用,结合反应的方程式计算.
解答:
解:(1)碳在高温下还原二氧化硅即得到粗硅,所以用滤渣制备粗硅的化学反应方程式为:2C+SiO2
Si+2CO↑,故答案为:2C+SiO2
Si+2CO↑;
(2)a.非金属性:C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:H2CO3>H2SiO3,故a正确;
b.酸性越弱,相应的酸根越容易结合氢离子,则结合质子的能力大小为:AlO2->CO32->HCO3-,故b错误;
c.非金属性O>C>Si,元素的非金属性越强,对应的氢化物越稳定,故c正确;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小,则O2->Al3+,故d错误;
故答案为:ac;
(3)滤渣中含有二氧化硅,所以滤渣和NaOH溶液反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;
如果含有氧化铝,则滤液中含有偏铝酸钠,偏铝酸钠能和CO2反应生成白色沉淀氢氧化铝,据此可以判断,即无色溶液中通入CO2无白色沉淀生成,证明不含氧化铝,
故答案为:SiO2+2OH-=SiO32-+H2O;无色溶液中通入CO2无白色沉淀生成;
(4)矿石含有FeCO3,可与HNO3发生氧化还原反应,反应的离子方程式为:3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O,
故答案为:3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O;
(5)由于NO是有毒气体,不能随意排放,所以这样做的目的是NO循环使用能减少环境污染,且NO跟H2O、O2反应后又得到硝酸提高原料利用率;
根据以上分析可知,该矿石中含有碳酸亚铁和二氧化硅,其中碳酸亚铁的质量是:2.36×103 kg-1.2×103 kg=1.16×103kg,
碳酸亚铁物质的量为
=10000mol,
则根据3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O可知,消耗硝酸的物质的量为:n(HNO3)=
n(FeCO3)=
mol≈3.33×104mol,
所以理论上至少需要1molL-1 HNO3的体积为:
=3.33×104L,
故答案为:NO循环使用能减少环境污染;NO跟H2O、O2反应后又得到硝酸提高原料利用率;3.33×104.
| ||
| ||
(2)a.非金属性:C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:H2CO3>H2SiO3,故a正确;
b.酸性越弱,相应的酸根越容易结合氢离子,则结合质子的能力大小为:AlO2->CO32->HCO3-,故b错误;
c.非金属性O>C>Si,元素的非金属性越强,对应的氢化物越稳定,故c正确;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小,则O2->Al3+,故d错误;
故答案为:ac;
(3)滤渣中含有二氧化硅,所以滤渣和NaOH溶液反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;
如果含有氧化铝,则滤液中含有偏铝酸钠,偏铝酸钠能和CO2反应生成白色沉淀氢氧化铝,据此可以判断,即无色溶液中通入CO2无白色沉淀生成,证明不含氧化铝,
故答案为:SiO2+2OH-=SiO32-+H2O;无色溶液中通入CO2无白色沉淀生成;
(4)矿石含有FeCO3,可与HNO3发生氧化还原反应,反应的离子方程式为:3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O,
故答案为:3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O;
(5)由于NO是有毒气体,不能随意排放,所以这样做的目的是NO循环使用能减少环境污染,且NO跟H2O、O2反应后又得到硝酸提高原料利用率;
根据以上分析可知,该矿石中含有碳酸亚铁和二氧化硅,其中碳酸亚铁的质量是:2.36×103 kg-1.2×103 kg=1.16×103kg,
碳酸亚铁物质的量为
| 1.16×106g |
| 116g/mol |
则根据3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O可知,消耗硝酸的物质的量为:n(HNO3)=
| 10 |
| 3 |
| 105 |
| 3 |
所以理论上至少需要1molL-1 HNO3的体积为:
| 3.33×104mol |
| 1mol/L |
故答案为:NO循环使用能减少环境污染;NO跟H2O、O2反应后又得到硝酸提高原料利用率;3.33×104.
点评:该题综合考查粗硅的制备、元素周期律的应用、物质的检验及有关计算等知识,是高考中的常见题型,题目难度较大,试题综合性强,侧重对学生能力的培养和解题方法的指导,有助于培养学生逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力;该试题还通过鼓励学生去大胆的猜想及拓展探究实验,考查学生的基本科学素养.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3Cl2+8NH3=6NH4Cl+N2的反应中,被氧化的NH3与未被氧化的NH3的分子数之比为( )
| A、1:6 | B、3:1 |
| C、1:3 | D、6:1 |
对于相同物质的量的SO2和SO3,下列说法正确的是( )
| A、氧元素的质量比为1:1 |
| B、SO2和SO3的质量比为1:1 |
| C、原子总数之比为1:1 |
| D、分子数之比为1:1 |
下列物质水溶液能导电,但是属于非电解质的是( )
| A、NH3 |
| B、(NH4)2SO4 |
| C、Cl2 |
| D、Na2O |
下列有关有机实验的叙述正确的是( )
| A、实验室制取乙烯时,应把无水乙醇与3mol/L的H2SO4混合均匀后迅速升温至170℃ |
| B、分馏操作中,温度计水银球应放置在蒸馏烧瓶支管口附近 |
| C、除去乙酸乙酯中乙酸杂质的方法是加入饱和NaOH溶液,充分振荡、静置后,分液 |
| D、检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |