题目内容
18.运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.(1)已知:$\frac{1}{2}$O2(g)═$\frac{1}{2}$O2+(g)+$\frac{1}{2}$e-△H1=+587.9kJ/mol K1
PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ/mol K2
O2+PtF6-(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ/mol K3
则反应O2(g)+PtF6(g)═O2+PtF6-(s)的△H=-77.5kJ/mol,K=$\frac{{{K}_{1}}^{2}•{K}_{2}}{{K}_{3}}$(用K1、K2、K3表示)
(2)一定条件下,铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),已知该反应的平衡常数K 与温度T 的关系如图甲所示.
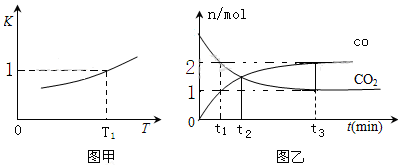
①T℃、p Pa压强下的密闭容器中进行反应,下列能说明反应达到平衡状态的是ad.
a.混合气体的平均相对分子质量不再变化
b.容器内压强不再变化
c.v正(CO2)=v逆 (FeO)
d.CO2的体积分数不再变化
②T1温度下,向体积为VL的密闭容器中加入足量铁粉并充入一定量的CO2,达到平衡时则CO2的平衡转化率为50%;反应过程中体系的能量增多(增多或降低)
③T2温度下,恒容密闭容器中,反应过程中测定CO和CO2物质的量与时间的关系如图乙所示.则T1>T2(填>、<或=),CO2的平衡转化率为66.7%,平衡时混合气体的密度与起始时气体的密度之比为25:33.
分析 (1)已知:①$\frac{1}{2}$O2(g)═$\frac{1}{2}$O2+(g)+$\frac{1}{2}$e-△H1=+587.9kJ/mol K1
②PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ/mol K2
③O2+PtF6-(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ/mol K3
根据盖斯定律:①×2÷②-③可得O2(g)+PtF6(g)═O2+PtF6-(s),据此计算;
(2)①当反应达到平衡状态时,正、逆反应速率相等(同种物质),各物质的浓度、含量不再改变,以及由此衍生的一些物理量也不变,以此进行判断;
②T1温度下反应的平衡常数为1,结合平衡三段式列式计算,转化率=$\frac{转化量}{起始量}$×100%计算;反应放热,体系能量增多;
③计算T2温度下的K,与T1的K比较可得,结合平衡三段式列式计算,转化率=$\frac{转化量}{起始量}$×100%计算转化率,平衡时混合气体的密度与起始时气体的密度之比为气体摩尔质量之比.
解答 解:(1)已知:①$\frac{1}{2}$O2(g)═$\frac{1}{2}$O2+(g)+$\frac{1}{2}$e-△H1=+587.9kJ/mol K1
②PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ/mol K2
③O2+PtF6-(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ/mol K3
根据盖斯定律:①×2÷②-③可得O2(g)+PtF6(g)═O2+PtF6-(s),△H=-77.5kJ/mol,K=$\frac{{{K}_{1}}^{2}•{K}_{2}}{{K}_{3}}$;
故答案为:-77.5kJ/mol;$\frac{{{K}_{1}}^{2}•{K}_{2}}{{K}_{3}}$;
(2)①Fe(s)+CO2(g)?FeO(s)+CO(g),反应前后是气体体积不变的放热反应,
a、反应前后气体物质的量不变,气体质量发生变化,混合气体的平均相对分子质量不再变化,说明反应达到平衡状态,a正确;
b、反应前后气体体积不变,容器内压强始终不发生变化,不能说明反应达到平衡状态,故b错误;
c、氧化亚铁是固体,不能表示反应速率,故c错误;
d、随着反应的进行,CO2的量减少,当体积分数不再变化达平衡状态,故d正确;
故答案为:ad;
②T1温度下,向体积为V L的密闭容器中加入足量铁粉并充入一定量的CO2,平衡常数为1,设二氧化碳起始量为x,变化量为y,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量 x 0
变化量 y y
平衡量 x-y y
平衡常数K=$\frac{y÷V}{(x-y)÷V}$=1,解得$\frac{y}{x}$=0.5=50%;反应放热,反应过程体系能量增多;
故答案为:50%;增多;
③根据图乙,设反应容器容积为V L,则K2=$\frac{2÷V}{1÷V}$=2,反应放热,化学平衡常数增大,说明反应温度降低,T1>T2;T2温度下,设反应容器容积为V L,平衡常数为2,设二氧化碳起始量为a,变化量为b,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量 a 0
变化量 b b
平衡量 a-b b
平衡常数K=$\frac{b÷V}{(a-b)÷V}$=2,解得:$\frac{b}{a}$=$\frac{2}{3}$=66.7%;平衡时混合气体的密度与起始时气体的密度之比为气体摩尔质量之比$\frac{44(a-b)+28b}{a}$:44=25:33;
故答案为:>; 66.7%; 25:33.
点评 本题考查了化学平衡图象分析,影响因素判断,热化学方程式书写,混合物反应的计算,题目难度中等,涉及焓变、反应热、物质的量的计算,试题计算量较大,充分考查学生的分析、理解能力及化学计算能力,明确发生反应的原理为解答关键.

| 方法1 | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
| 方法2 | 用水煤气(主要成分为CO、H2等)将SO2在高温下还原成单质硫 |
| 方法3 | 用Na2SO3溶液吸收SO2转化为NaHSO3,再经电解转化为H2SO4 |
A.适当增大氨水浓度 B.使燃煤烟气与氨水充分接触
C.向氨水中加入少量硫酸 D.把氨水加热至100℃
(2)方法2中主要发生了下列反应:
①2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+8.0KJ•mol-1
②2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4KJ•mol-1
该方法从能量转化的角度,可看作由热能转化为化学能.
(3)方法3可用甲烷燃料电池作为电源,对吸收SO2后的NaHSO3溶液进行电解实验,如图所示.回答下列问题:
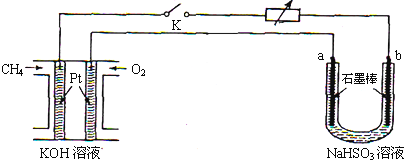
①甲烷燃料电池中,通入CH4(填“CH4”或“O2”)的一极为负极;正极的电极反应式为O2+4e-+2H2O=4OH-;该电池放电后,溶液的碱性会减弱(填“增强”,“减弱”或“不变”).
下列关于该燃料电池的说法中不正确的是B.
A.该燃料电池可把化学能直接转变为电能
B.该燃料电池中化学能100%转变为电能
C.该燃料电池的优点之一是无污染,是一种具有应用前景的绿色电源
②a电极的名称是阳极;闭合开关K后,b电极上发生的反应类型是还原反应.
③若上述甲烷燃料电池中用的是200mL 0.10mol•L-1的KOH溶液,闭合开关K一段时间后,测得U形管中生成了0.02molSO42-.试计算此时燃料电池中KOH的物质的量浓度(假设反应前后溶液的体积不变,列出计算过程).
| A. | c(H+)•c(OH-)=KW | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)+c(OH-) | D. | c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
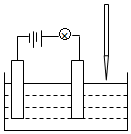 在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A. | 醋酸中逐滴加入氢氧化钠溶液 | B. | 硫酸钠中逐滴加入氢氧化钡溶液 | ||
| C. | 硫酸中逐滴加入氢氧化钡溶液 | D. | 盐酸中逐滴加入硝酸银溶液 |
| A. | 为了节约应将实验过程中取用的剩余药品放回原试剂瓶 | |
| B. | 在汽油罐上所贴的危险化学品标志内容是:遇湿易燃物品 | |
| C. | 酒精着火,迅速用湿抹布或沙子盖灭 | |
| D. | 氢氧化钠溶液溅入眼中,应立即用大量水冲洗,再用稀盐酸冲洗 |
| A. | CH3CH(CH3)CH2CH3 2-甲基丁烷 | B. | 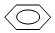 间二甲苯 间二甲苯 | ||
| C. | CH3CH2CH2CH2OH 1-羟基丁烷 | D. | 2-甲基-2-丙烯 |
 H2SO32H2SO3+O2
H2SO32H2SO3+O2 2H2SO4.
2H2SO4. 2SO3反应的△H=-198kJ/mol,是放热反应.当压强一定时,温度升高,平衡左移,SO2平衡转化率减小.
2SO3反应的△H=-198kJ/mol,是放热反应.当压强一定时,温度升高,平衡左移,SO2平衡转化率减小.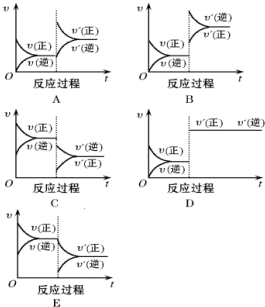
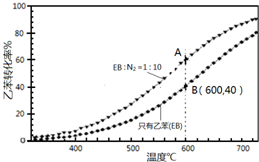 苯乙烯(
苯乙烯(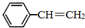 )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得: CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$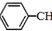 =CH2(g)+H2(g)△=+QkJ.mol-1
=CH2(g)+H2(g)△=+QkJ.mol-1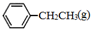 、
、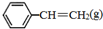 、H2(g)的燃烧热(△H)分别为-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,写出Q与Q1、Q2、Q3的关系式Q2+Q3-Q1.
、H2(g)的燃烧热(△H)分别为-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,写出Q与Q1、Q2、Q3的关系式Q2+Q3-Q1.