题目内容
4.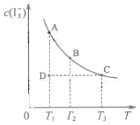 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )| A. | 反应 I2(aq)+I-(aq)?I3-(aq)△H>0 | |
| B. | 状态A与状态B相比,状态A的c(I2)大 | |
| C. | 若反应进行到状态D时,一定有v逆>v正 | |
| D. | 若温度为T1、T2,反应的平衡常数K1、K2则 K1>K2 |
分析 由图象曲线的变化趋势可知,当温度升高时,I3-的物质的量浓度减小,说明平衡向逆反应方向移动,该反应的正反应为放热反应;升高温度,平衡向逆反应方向移动,温度越高,平衡常数越小,从温度对平衡移动的影响分别判断碘单质的转化率、平衡常数的变化、反应进行方向及不同状态的A的浓度大小,以此解答.
解答 解:A.由图象曲线的变化趋势可知,当温度升高时,I3-的物质的量浓度减小,说明该反应的正反应为放热反应,反应I2(aq)+I-(aq)?I3-(aq)的△H<0,故A错误;
B.温度升高,平衡向逆方向移动,c(I3-)变小,则c(I2)应变大,所以状态B的c(I2)大,故B错误;
C.若反应进行到状态D时,反应未达到平衡状态,若反应趋向于平衡,则反应向生成的I3-方向移动,则v正>v逆,故C错误;
D.该反应的正反应为放热反应,升高温度,平衡向逆反应方向移动,温度越高,平衡常数越小,若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2,故D正确.
故选D.
点评 本题考查化学平衡移动图象问题,为高频考点,题目难度中等,注意根据图象曲线变化分析化学方程式的特征以及温度、浓度、压强对平衡移动的影响,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.①pH=3的CH3COOH溶液;②PH=3的HCl溶液;③PH=11的氨水;④pH=11的NaOH溶液.相同条件下,有关上述溶液的比较中,正确的是( )
| A. | 水电离产生的c(H+):①=③>④=② | |
| B. | 将②、③溶液混合后,pH=7,消耗溶液的体积:②>③ | |
| C. | 等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量;②最大 | |
| D. | 向溶液中加入100mL水后,溶液的pH:③>④>①>② |
16.骨架分类,下列说法正确的是( )
| A. | 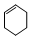 属于芳香族化合物 属于芳香族化合物 | B. |  属于苯的同系物 属于苯的同系物 | ||
| C. |  属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2属于链状化合物 |
13.在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+下列判断正确的是( )
| A. | 高锰酸钾是氧化剂,Na2O2既是氧化剂,又是还原剂 | |
| B. | 反应的氧化产物Mn2+ | |
| C. | 当反应产生标准状况下2.24L O2 时,反应转移的电子为0.2mol | |
| D. | 向高锰酸钾溶液滴加浓盐酸可以得到酸性高锰酸钾溶液 |
 HCl溶液的pH=____________;0.01 mol/L NaOH溶液的pH=______________;pH=11的CH3COONa溶液中由水电离产生的c(OH-) =___________。
HCl溶液的pH=____________;0.01 mol/L NaOH溶液的pH=______________;pH=11的CH3COONa溶液中由水电离产生的c(OH-) =___________。