题目内容
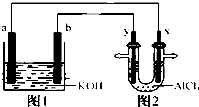 已知有如图装置,a为Mg、b为Al,图2电极材料均为石墨,下列说法正确的是( )
已知有如图装置,a为Mg、b为Al,图2电极材料均为石墨,下列说法正确的是( )| A、b和y表面均冒氢气,b对应电极反应式:6H2O+6e-=3H2↑+6OH- |
| B、装置图1工作时电解质溶液PH将增大 |
| C、将装置图1电解质溶液改成硝酸钾和硫酸氢钠混合溶液则装置图1中产生无色气体后在液面上方气体变红棕色 |
| D、当图2装置中产生0.1mol白色沉淀时x,y处共产生气体6.72L |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:图1为原电池,Al易失电子作负极、Mg作正极,负极反应式为Al-3e-+4OH-═AlO2-+2H2O,正极反应式为6H2O+6e-=6OH-+3H2↑;图2为电解池,x为阳极、y为阴极,阳极上电极反应式为2Cl-2e-=Cl2↑、2H2O+2e-=2OH-+H2↑,溶液中还发生反应2Al3++3OH-=Al(OH)3↓,据此分析解答.
解答:
解:A.b电极反应式为Al-3e-+4OH-═AlO2-+2H2O、y电极反应式为2H2O+2e-=2OH-+H2↑,所以b电极上没有气体生成,故A错误;
B.图1电池反应式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,该反应中NaOH参加反应,导致溶液碱性减弱,pH减小,故B错误;
C.将装置图1电解质溶液改成硝酸钾和硫酸氢钠混合溶液,溶液中相当于含有硝酸,硝酸和金属Mg反应生成NO,NO不稳定,易被氧气氧化生成红棕色气体二氧化氮,所以装置图1中产生无色气体后在液面上方气体变红棕色,故C正确;
D.根据2Al3++3OH-=Al(OH)3↓知,生成0.1mol白色沉淀需要0.3molOH-,根据 2H2O+2e-=2OH-+H2↑知,生成0.3molOH-需要0.3mol电子,串联电路中转移电子相等,根据2H2O+2e-=2OH-+H2↑知,转移0.3mol电子生成0.15mol氢气,体积=0.15mol×22.4L/mol=3.36L,故D错误;
故选C.
B.图1电池反应式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,该反应中NaOH参加反应,导致溶液碱性减弱,pH减小,故B错误;
C.将装置图1电解质溶液改成硝酸钾和硫酸氢钠混合溶液,溶液中相当于含有硝酸,硝酸和金属Mg反应生成NO,NO不稳定,易被氧气氧化生成红棕色气体二氧化氮,所以装置图1中产生无色气体后在液面上方气体变红棕色,故C正确;
D.根据2Al3++3OH-=Al(OH)3↓知,生成0.1mol白色沉淀需要0.3molOH-,根据 2H2O+2e-=2OH-+H2↑知,生成0.3molOH-需要0.3mol电子,串联电路中转移电子相等,根据2H2O+2e-=2OH-+H2↑知,转移0.3mol电子生成0.15mol氢气,体积=0.15mol×22.4L/mol=3.36L,故D错误;
故选C.
点评:本题考查原电池和电解池原理,正确书写各个电极反应式是解本题关键,注意不能根据金属活泼性强弱判断正负极,易错选项是C,如果将NaOH溶液换为硝酸钾和硫酸氢钠混合溶液,实际上相当于溶液中含有硝酸,很多同学往往认为是硫酸起作用而导致错误,为易错点.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
表示下列过程的化学用语正确的是( )
| A、明矾可用于净水:Al3++3H2O?Al(OH)3↓+3H+ |
| B、亚硫酸氢钠溶液显酸性:NaHSO3?Na++H++SO32- |
| C、碳酸氢钙溶液和足量的氢氧化钠溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D、向明矾溶液中逐滴加入氢氧化钡溶液使Al3+沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A、H+、I-、Br2、Na+ |
| B、Ag+、NO3-、Cl-、K+ |
| C、K+、Ba2+、OH-、SO42- |
| D、Cu2+、NH4+、Br-、OH- |
下列说法中正确的是( )
| A、1mol/L的NaCl溶液是指此溶液中含有1mol NaCl |
| B、从1 L 0.5 mol/L的NaCl溶液中取出100 mL溶液,其物质的量浓度变为0.1 mol/L |
| C、常温下,1molCl2的体积约为22.4L |
| D、l mol/L的CaCl2溶液中,Cl-的物质的量浓度为2 mol/L |
下列实验能达预期目标的是( )
①用饱和Na2CO3溶液除去乙酸乙酯中少量的乙酸、乙醇
②将Cl2直接通入品红溶液,品红褪色证明Cl2有漂白性
③用食醋和澄清石灰水验证蛋壳中含有CO32-
④用硝酸钡溶液鉴别SO42-、SO32-
⑤用酸性高锰酸钾溶液检验苯分子中是否存在类似烯烃的碳碳双键.
①用饱和Na2CO3溶液除去乙酸乙酯中少量的乙酸、乙醇
②将Cl2直接通入品红溶液,品红褪色证明Cl2有漂白性
③用食醋和澄清石灰水验证蛋壳中含有CO32-
④用硝酸钡溶液鉴别SO42-、SO32-
⑤用酸性高锰酸钾溶液检验苯分子中是否存在类似烯烃的碳碳双键.
| A、①②③ | B、①③⑤ |
| C、①②⑤ | D、②④⑤ |
下列关于能量转换的认识中,不正确的是( )
| A、白炽灯工作时,电能转化为化学能 |
| B、绿色植物进行光合作用时,太阳能转化为化学能 |
| C、电解水生成氢气和氧气,电能转化为化学能 |
| D、煤燃烧时化学能主要转化为热能 |
用铝粉和碘甲烷制取(CH3)3Al时,于100℃搅拌65h,产率为0.若用超声波,则在室温下2.5h,产率可达96%.下列有关叙述正确的是( )
| A、超声波加快反应速率的作用大于搅拌 |
| B、超声波使铝粉在碘甲烷中乳化成为胶体 |
| C、超声波使反应物局部急剧升温 |
| D、超声波使碘甲烷分解为碘和甲烷的速率加快 |
下列说法正确的是( )
| A、ⅦA族元素非金属性比ⅥA族元素非金属性强 |
| B、在多电子的原子中,能量高的电子通常离核近的区域内运动 |
| C、周期表中,在过渡元素区域寻找各种优良的催化剂 |
| D、物质中原子或离子间的相互作用都是化学键 |
下列说法不正确的是( )
| A、物质的量是用来研究微观粒子的一个国际基本物理量,其单位是摩尔 |
| B、气体的摩尔体积与温度和压强有关,压强越大,体积越大 |
| C、若x个N(氮)原子的质量是1克,则阿佛加德罗常数可表示为28x/mol |
| D、任何一种微观粒子,当摩尔质量以g/mol为单位时,其数值与这种粒子的相对分子质量或相对原子质量相同 |