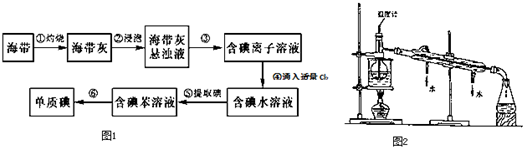
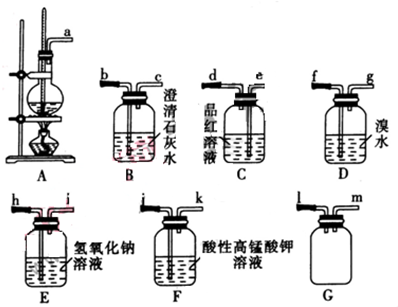
题目内容
 研究NO2、SO2、NO、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、NO、CO等大气污染气体的处理具有重要意义.(1)已知:S(s)+O2(g)=SO2(g)△H=-297.0kJ/mol,2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol,写出将SO2和CO转化为S(s)和CO2的热化学方程式
(2)研究发现NO2、SO2可按如下反应处理:NO2(g)+SO2(g)?NO(g)+SO3(g)△H,在恒温恒容的条件下,将NO2与SO2的混合气体置于密闭容器中发生上述反应.
①若升高温度,发现混合气体颜色变深,说明该反应的正反应为
②下列情况能说明该反应已经达到平衡状态的是
A.各物质的量浓度不再发生变化 B.每消耗1mol NO2的同时生成1mol SO3
C.混合气体的平均相对分子质量不再发生变化 D.NO和SO3的体积比保持不变
③反应达到平衡后,往容器中通入一定体积的He,平衡将
(3)新的催化技术可将NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.如图2表示在密闭容器中发生上述反应,达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况.
①a~b过程中改变的条件可能是
②b~c过程中改变的条件可能是
③若保持容器体积不变,在c时刻时继续通入一定体积的NO和CO,将反应速率的变化情况画在c~d处.
考点:用盖斯定律进行有关反应热的计算,化学平衡状态的判断,化学反应速率与化学平衡图象的综合应用
专题:化学反应中的能量变化,化学平衡专题
分析:(1)利用盖斯定律,抵消中间产物,得到目的反应同时计算△H,书写热化学方程式;
(2)①颜色加深,说明二氧化氮的含量增加,平衡向着生成二氧化氮的方向移动;
②根据可逆反应达到平衡状态时,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化,该反应中只有二氧化氮为有色气体、正反应为气体体积减小的反应,据此进行判断;
③充入稀有气体,对各组分浓度没有影响,化学平衡不会变化;
(3)利用影响化学反应速率及化学平衡的因素来分析;根据正逆反应速率的变化结合、催化剂、温度、压强对反应速率和化学平衡的影响判断;根据化学方程式的特征,结合外界条件对平衡移动的影响分析图象的曲线变化趋势.
(2)①颜色加深,说明二氧化氮的含量增加,平衡向着生成二氧化氮的方向移动;
②根据可逆反应达到平衡状态时,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化,该反应中只有二氧化氮为有色气体、正反应为气体体积减小的反应,据此进行判断;
③充入稀有气体,对各组分浓度没有影响,化学平衡不会变化;
(3)利用影响化学反应速率及化学平衡的因素来分析;根据正逆反应速率的变化结合、催化剂、温度、压强对反应速率和化学平衡的影响判断;根据化学方程式的特征,结合外界条件对平衡移动的影响分析图象的曲线变化趋势.
解答:
解:(1)已知:①S(s)+O2(g)=SO2(g)△H=-297.0kJ/mol,②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol,根据盖斯定律:①+②得SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-269.0kJ/mol,
故答案为:SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-269.0kJ/mol;
(2)①当温度升高时,混合气体颜色变深,说明反应物二氧化氮的浓度增大,平衡向着逆向移动,逆反应为吸热反应,正反应为放热反应,故答案为:放热;
②NO2(g)+SO2(g)?NO(g)+SO3(g)
A.各物质的量浓度不再发生变化,说明正逆反应速率相等,达到了平衡状态,故A正确;
B.每消耗1molNO2的同时生成1mol SO3只能表明化学反应正向进行,不能体现正逆反应速率相等,故B错误;
C.混合气体的平均相对分子质量不再发生变化,该反应是一个反应前后气体体积相等的化学反应,反应前后气体的物质的量不变,质量守恒,所以混合气体的摩尔质量始终不变,所以不能根据混合气体的平均相对分子质量不再变化来判断平衡状态,故C错误;
D.NO和SO3的体积比保持不变,只能表明化学反应正向进行,这与反应的转化程度无关,不能确定是否达到平衡,故D错误;
故选A;
③向容器中通入稀有气体He,由于反应体系中各组分浓度没有变化,化学平衡不会移动,故答案为:不;
(3)①a时正逆反应速率都增大,可能为增大压强或者升高温度或使用催化剂,且逆反应速率等于正反应速率,平衡不移动,若最大压强平衡正向移动,弱升高温度,平衡向着逆向移动,所以使用催化剂平衡不移动满足条件;
故答案为:使用催化剂;
②b时是正反应速率减小,逆反应速率减小,正反应速率小于逆反应速率,平衡向着逆向移动,应为减小压强的原因,
故答案为:减小压强;
③化学方程式如下:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0,若保持容器体积不变,在c时刻时继续通入一定体积的NO和CO,反应物浓度增大,生成物浓度瞬间不变,且平衡向正反应方向移动,所以图象如图: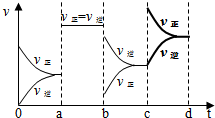 ,故答案为:
,故答案为: .
.
故答案为:SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-269.0kJ/mol;
(2)①当温度升高时,混合气体颜色变深,说明反应物二氧化氮的浓度增大,平衡向着逆向移动,逆反应为吸热反应,正反应为放热反应,故答案为:放热;
②NO2(g)+SO2(g)?NO(g)+SO3(g)
A.各物质的量浓度不再发生变化,说明正逆反应速率相等,达到了平衡状态,故A正确;
B.每消耗1molNO2的同时生成1mol SO3只能表明化学反应正向进行,不能体现正逆反应速率相等,故B错误;
C.混合气体的平均相对分子质量不再发生变化,该反应是一个反应前后气体体积相等的化学反应,反应前后气体的物质的量不变,质量守恒,所以混合气体的摩尔质量始终不变,所以不能根据混合气体的平均相对分子质量不再变化来判断平衡状态,故C错误;
D.NO和SO3的体积比保持不变,只能表明化学反应正向进行,这与反应的转化程度无关,不能确定是否达到平衡,故D错误;
故选A;
③向容器中通入稀有气体He,由于反应体系中各组分浓度没有变化,化学平衡不会移动,故答案为:不;
(3)①a时正逆反应速率都增大,可能为增大压强或者升高温度或使用催化剂,且逆反应速率等于正反应速率,平衡不移动,若最大压强平衡正向移动,弱升高温度,平衡向着逆向移动,所以使用催化剂平衡不移动满足条件;
故答案为:使用催化剂;
②b时是正反应速率减小,逆反应速率减小,正反应速率小于逆反应速率,平衡向着逆向移动,应为减小压强的原因,
故答案为:减小压强;
③化学方程式如下:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0,若保持容器体积不变,在c时刻时继续通入一定体积的NO和CO,反应物浓度增大,生成物浓度瞬间不变,且平衡向正反应方向移动,所以图象如图:
 ,故答案为:
,故答案为: .
.
点评:本题综合考查了反应速率、反应方向、化学平衡等知识,并注重考查了化学反应速率与化学平衡图象的综合应用,充分体现了新课程变化,同时又注重了对高考热点的考查,注意充入稀有气体,对平衡没有影响,注意把握化学方程式的特征,结合外界条件对平衡移动的影响分析图象的曲线变化趋势,题目难度中等.

练习册系列答案
相关题目
欲增加Mg(OH)2在水中的溶解度,可采用的方法是( )
| A、增加溶液pH |
| B、加入2.0mol?L-1 NH4Cl |
| C、加入0.1mol?L-1 MgSO4 |
| D、加入适量95%乙醇 |
某同学根据苯和四氯化碳互溶、苯的密度比水小、四氯化碳的密度比水大的性质制作了“液体积木”.在试管中注入四氯化碳,再加少量水,再小心加入少量苯,溶液可出现分三层的现象,然后再用漏斗向水层中加入少量胆矾溶液及少量碘水.下列说法正确的是( )
| A、不振荡,静置后上中下三层的颜色分别为无色、蓝色、紫色 |
| B、不振荡,静置后上中下三层的颜色分别为紫色、蓝色、紫色 |
| C、振荡,静置后溶液分为两层,水在下层 |
| D、振荡,静置后溶液仍分为三层 |
 饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一.某兴趣小组进行了如下实验探究:
饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一.某兴趣小组进行了如下实验探究:①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;第二份与稀盐酸混合,立即产生大量无色气体;第三份滤液加热,看到滤液变浑浊且有大量无色气体产生.经检测,上述实验中产生的无色气体均为CO2.依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有( )
| A、Ca(ClO)2 |
| B、CaCO3 |
| C、Ca(HCO3)2 |
| D、CaO |