题目内容
一种新型镁铝合金的化学式为Mg17Al12,它具有储氢性能,该合金在一定条件下完全吸氢的化学方程式为:Mg17Al12+17H2=17MgH2+12Al,得到的混合物Y(17MgH2+12Al)在一定条件下能释放出氢气。下列说法正确的是
A.该合金的熔点介于金属镁和金属铝熔点之间
B.该合金中镁元素呈负价,铝元素呈正价
C.1mol Mg17Al12完全吸氢后得到的混合物Y与盐酸完全反应释放出H2,若消耗盐酸的体积为14L,则该盐酸的物质的量浓度为5mol.L-1
D.制备该合金应在氮气保护下,将一定比例的Mg、Al单质在一定温度下熔炼而获得
C
【解析】
试题分析:A.该合金的熔点应该低于成分金属的熔点,错误;B.在合金中镁元素、铝元素都是以单质形式存在,化合价都是0价,错误;C.1mol Mg17Al12完全吸氢后得到的混合物Y与盐酸完全反应释放出H2,若消耗盐酸的体积为14L,根据元素守恒,可得消耗盐酸的物质的量是17×2+12×3=70mol,则该盐酸的物质的量浓度为70mol ÷14L=5mol.L-1 ,正确;D.由于Mg是活泼的金属,容易与氮气发生反应,所以若制备该合金应在氮气作用下不能制取获得,错误。
考点:考查新型镁铝合金的制取、性质及应用的知识。

练习册系列答案
相关题目

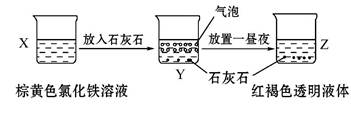
 +2Fe3++3H
+2Fe3++3H O====2Fe(OH)3+3CO
O====2Fe(OH)3+3CO ↑+3Ca2+
↑+3Ca2+