题目内容
12.在甲酸的下列性质中,可以证明它是弱电解质的是( )| A. | 1mol/L的甲酸溶液中c(H+)约为0.01mol/L | |
| B. | 甲酸与水以任意比例互溶 | |
| C. | 10mL 1mol/L的甲酸溶液恰好与10mL 1mol/L的NaOH溶液完全反应 | |
| D. | 在相同温度下,物质的量浓度相同的甲酸导电性比硫酸弱 |
分析 A.甲酸是弱电解质,不能完全电离;
B.甲酸与水以任意比例互溶,这是甲酸的物理性质,不能证明是弱电解质;
C.是中和反应,按照反应方程式进行;
D.硫酸是二元强酸.
解答 解:A.1mol•L-1的甲酸溶液的c(H+)约为0.01mol•L-1说明甲酸不能完全电离,可以证明是弱电解质,故A正确;
B.甲酸水溶性是物理性质,不能证明是弱电解质;
C.根据方程式可知不论酸碱强弱,只有一元酸与一元碱物质的量相等则恰好发生酸碱中和,完全反应,故C错误;
D.由于硫酸是二元强酸,故在相同温度下,即使甲酸是强电解质,相同浓度时其导电能力也比硫酸的弱,故不能说明甲酸是弱电解质,故D错误.
故选A.
点评 本题考查了弱电解质的判断,题目难度不大,注意把握住弱电解质的定义“部分电离”的特点.

练习册系列答案
相关题目
3.下列各类有机物:①饱和一元醇 ②饱和一元醛 ③饱和一元羧酸 ④饱和一元醇与饱和一元酸生成的酯 ⑤乙炔的同系物 ⑥苯的同系物 ⑦烯烃的同系物,完全燃烧时产生的水和二氧化碳的物质的量之比恒定的是( )
| A. | ①③⑤⑦ | B. | ①④⑥ | C. | ②③④⑦ | D. | ②③④⑤⑥ |
20.下列递变规律正确的是( )
| A. | O、S、Na、K的原子半径一次增大 | |
| B. | Na、Mg、Al、Si的金属性逐渐增强 | |
| C. | HF、HCl、HBr、HI的沸点依次增高 | |
| D. | KOH、Ca(OH)2、Mg(OH)2、Al(OH)3的碱性逐渐增强 |
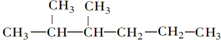 2,3-二甲基己烷;
2,3-二甲基己烷;