题目内容
甲醇(CH3OH)是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g)?CH3OH(g)
t℃时,往1L密闭容器中充入1mol CO和2molH2.10min后,反应达到平衡,并测得CH3OH(g)的浓度为0.8mol?L-1.
(1)①该时间内反应速率v(H2)= .t℃时,该反应的化学平衡常数K= (mol?L-1)-2
②下列各项中,能说明该反应已达到平衡的是 (填序号)
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,测得v正(CO)=v逆(CH3OH)
c.恒温、恒容条件下,容器内的气体密度不发生变化
d.一定条件下,单位时间内消耗2mol H2,同时生成1mol CH3OH(g)
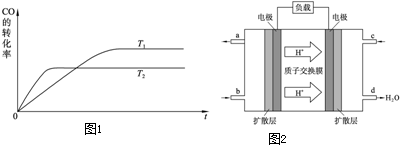
(2)如图1是该反应在T1、T2温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H 0(填“>”、“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1 K2(填“>”、“<”或“=”).
③若保持容器容积不变,下列措施可增加甲醇产率的是 .
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H= kJ?mol-1.
(4)我国在甲醇燃料电池技术方面已获得重大突破.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,b口通入的物质为 .
②该电池正极的电极反应式为 .
CO(g)+2H2(g)?CH3OH(g)
t℃时,往1L密闭容器中充入1mol CO和2molH2.10min后,反应达到平衡,并测得CH3OH(g)的浓度为0.8mol?L-1.
(1)①该时间内反应速率v(H2)=
②下列各项中,能说明该反应已达到平衡的是
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,测得v正(CO)=v逆(CH3OH)
c.恒温、恒容条件下,容器内的气体密度不发生变化
d.一定条件下,单位时间内消耗2mol H2,同时生成1mol CH3OH(g)
(2)如图1是该反应在T1、T2温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H
②T1和T2温度下的平衡常数大小关系是K1
③若保持容器容积不变,下列措施可增加甲醇产率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=
(4)我国在甲醇燃料电池技术方面已获得重大突破.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,b口通入的物质为
②该电池正极的电极反应式为

考点:化学平衡的影响因素,用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理,化学平衡状态的判断
专题:
分析:(1)①根据三段式结合V=
,平衡常数指平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值进行计算;
②化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量不变,以此进行判断;
(2)①根据温度对化学平衡的影响来回答;
②温度对化学平衡常数的影响和反应的吸放热有关;
③化学平衡正向移动可增加甲醇产率;
(3)根据盖斯定律进行计算焓变;
(4)在甲醇燃料电池中,燃料甲醇作负极,发生失电子的氧化反应,氧气作正极,发生得电子的还原反应.
| △c |
| △t |
②化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量不变,以此进行判断;
(2)①根据温度对化学平衡的影响来回答;
②温度对化学平衡常数的影响和反应的吸放热有关;
③化学平衡正向移动可增加甲醇产率;
(3)根据盖斯定律进行计算焓变;
(4)在甲醇燃料电池中,燃料甲醇作负极,发生失电子的氧化反应,氧气作正极,发生得电子的还原反应.
解答:
解:(1)①可逆反应:CO(g)+2H2(g)?CH3OH(g)
开始 1 2 0
转化 0.8 1.6 0.8
平衡 0.2 0.4 0.8
所以该时间内反应速率v(H2)=
=0.16mol/(L?min)
平衡常数K=
=
=25,
故答案为:0.16mol/(L?min);25;
②a.反应前后气体的体积不等,恒温、恒容条件下,容器内的压强不发生变化,可说明达到平衡状态,故a正确;
b.一定条件下,因为反应速率之比等于系数之比,所以v正(CO)=v逆(CH3OH)=以v逆(CO),可说明正逆反应速率相等,达到平衡状态,故b正确;
c.气体的质量不变,容器的体积不变,无论是否达到平衡状态,都存在密度不变的特征,不能说明达到平衡状态,故c错误;
d.一定条件下,单位时间内消耗2mol H2,同时生成1molCH3OH,都指正反应方向,不能说明达到平衡状态,故d错误;
故答案为:a、b;
(2)①反应CO(g)+2H2(g)?CH3OH(g)中,反应向右进行,一氧化碳的转化率增大,温度升高,化学平衡向着吸热方向进行,根据图中的信息可以知道:T2>T1,所以该反应是放热反应,故答案为:<;
②对于放热反应,温度越高,化学平衡常数越小,T2>T1,反之越大,所以K1>K2,故答案为:>;
③a、若容器容积不变,升高温度,反应CO(g)+2H2(g)?CH3OH(g)平衡逆向移动,甲醇产率降低,故错误;
b、将CH3OH(g)从体系中分离,反应CO(g)+2H2(g)?CH3OH(g)平衡正向移动,甲醇产率增大,故正确;
c、使用合适的催化剂不会引起化学平衡的移动,甲醇的转化率不变,故错误;
d、若容器容积不变,充入He,使体系总压强增大,单质各组分的浓度不变,化学平衡不移动,甲醇的转化率不变,故错误;
故选b;
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
则(①-②)×
得,CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=
kJ?mol-1,故答案为:
;
(4)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以c口通入的物质为氧气,b口通入的物质为甲醇,故答案为:CH3OH;
②该电池正极是氧气发生得电子的还原反应,电极反应式为:O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O.
开始 1 2 0
转化 0.8 1.6 0.8
平衡 0.2 0.4 0.8
所以该时间内反应速率v(H2)=
| ||
| 10min |
平衡常数K=
| c(CH 3OH) |
| c(CO)?c 2(H 2) |
| 0.8 |
| 0.2×0.4 2 |
故答案为:0.16mol/(L?min);25;
②a.反应前后气体的体积不等,恒温、恒容条件下,容器内的压强不发生变化,可说明达到平衡状态,故a正确;
b.一定条件下,因为反应速率之比等于系数之比,所以v正(CO)=v逆(CH3OH)=以v逆(CO),可说明正逆反应速率相等,达到平衡状态,故b正确;
c.气体的质量不变,容器的体积不变,无论是否达到平衡状态,都存在密度不变的特征,不能说明达到平衡状态,故c错误;
d.一定条件下,单位时间内消耗2mol H2,同时生成1molCH3OH,都指正反应方向,不能说明达到平衡状态,故d错误;
故答案为:a、b;
(2)①反应CO(g)+2H2(g)?CH3OH(g)中,反应向右进行,一氧化碳的转化率增大,温度升高,化学平衡向着吸热方向进行,根据图中的信息可以知道:T2>T1,所以该反应是放热反应,故答案为:<;
②对于放热反应,温度越高,化学平衡常数越小,T2>T1,反之越大,所以K1>K2,故答案为:>;
③a、若容器容积不变,升高温度,反应CO(g)+2H2(g)?CH3OH(g)平衡逆向移动,甲醇产率降低,故错误;
b、将CH3OH(g)从体系中分离,反应CO(g)+2H2(g)?CH3OH(g)平衡正向移动,甲醇产率增大,故正确;
c、使用合适的催化剂不会引起化学平衡的移动,甲醇的转化率不变,故错误;
d、若容器容积不变,充入He,使体系总压强增大,单质各组分的浓度不变,化学平衡不移动,甲醇的转化率不变,故错误;
故选b;
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
则(①-②)×
| 1 |
| 2 |
| b-a |
| 2 |
| b-a |
| 2 |
(4)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以c口通入的物质为氧气,b口通入的物质为甲醇,故答案为:CH3OH;
②该电池正极是氧气发生得电子的还原反应,电极反应式为:O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O.
点评:本题考查较为综合,涉及反应速率、平衡常数的计算、平衡状态的判断、外界条件对平衡移动的影响以及盖斯定律的应用和燃料电池的原理等问题,题目难度中等,本题注意把握计算方法以及平衡常数的运用.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
利用下列反应不能制的括号中纯净物的是( )
| A、等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) |
| B、乙烯与水加成(乙醇) |
| C、乙烯与氯气加成(1,2-二氯乙烷) |
| D、氯气与苯用氯化铁作催化剂反应(氯苯) |
一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2,发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡后改变下述条件,SO3气体平衡浓度不改变的是( )
| A、保持温度和容器体积不变,充入1 mol SO3 |
| B、保持温度和容器压强不变,充入1 mol SO3 |
| C、保持温度和容器压强不变,充入1 mol O2 |
| D、保持温度和容器压强不变,充入1 mol Ar |
某溶液中由水电离的氢离子浓度是1×10-14mol/L,在此溶液中一定能大量共存的离子是( )
| A、Al3+、SO42-、NH4+、Cl- |
| B、K+、Fe2+、Cl-、NO3- |
| C、K+、Na+、Cl-、SO42- |
| D、Na+、K+、NO3-、HCO3- |

 第四周期过渡元素易与C、H、N、O形成多种化合物.
第四周期过渡元素易与C、H、N、O形成多种化合物. 中和热的测定实验的关键是 要比较准确地配制一定的物质的量浓度的溶液,在实验过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化.回答下列问题:
中和热的测定实验的关键是 要比较准确地配制一定的物质的量浓度的溶液,在实验过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化.回答下列问题: