题目内容
9.下列有关氢化物的叙述中正确的是( )| A. | 在卤化氢中HF最稳定 | B. | HCl的电子式为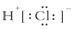 | ||
| C. | 一个D2O分子所含的中子数为8 | D. | 稳定性:H2S>HF |
分析 A.元素的非金属性越强,对应的氢化物越稳定;
B.HCl为共价化合物,电子式中不存在离子;
C.O的中子数为8,D的中子数为1;
D.元素的非金属性越强,对应的氢化物越稳定.
解答 解:A.卤族元素中,F的非金属性最强,则在卤化氢中HF最稳定,故A正确;
B.HCl为共价化合物,电子式中不存在离子,HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物其电子式为 ,故B错误;
,故B错误;
C.一个D2O分子所含的中子数为1×2+8=10,故C错误;
D.元素的非金属性越强,对应的氢化物越稳定,非金属性F>S,则稳定性为HF>H2S,故D错误;
故选A.
点评 本题考查氢化物的性质,明确非金属性越强,则气态氢化物越稳定是解答本题的关键,并熟悉原子的构成、化合物的种类等来解答,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
19.在无色透明的溶液中能大量共存的一组离子是( )
| A. | Cu2+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Na+、K+、OH-、Cl- | ||
| C. | Mg2+、Na+、OH-、SO${\;}_{4}^{2-}$ | D. | Ba2+、H+、CO${\;}_{3}^{2-}$、OH- |
20.下列说法正确的是( )
| A. | 石油分馏可以获得乙烯 | |
| B. | 煤经过气化和液化等物理变化可转化为淸洁燃料 | |
| C. | 聚乙烯塑料制品可用于食品包装 | |
| D. | 天然气和液化气的主要成分都是甲烷 |
1.M元素的阳离子与N元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径M<N;②离子半径M>N;③原子序数M>N;④原子最外层电子数M<N;⑤M的正价与N的负价绝对值一定相等;⑥元素所在的周期数:M>N;⑦元素的非金属性:M>N.
其中正确的组合是( )
①原子半径M<N;②离子半径M>N;③原子序数M>N;④原子最外层电子数M<N;⑤M的正价与N的负价绝对值一定相等;⑥元素所在的周期数:M>N;⑦元素的非金属性:M>N.
其中正确的组合是( )
| A. | ①②⑦ | B. | ③④⑤⑥⑦ | C. | ③⑤ | D. | ③④⑥ |
7.500mL NaNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体22.4L(标准状况下),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A. | 原混合溶液中c(Na+)=6 mol | |
| B. | 电解后得到的Cu的物质的量为2 mol | |
| C. | 上述电解过程中共转移8 mol电子 | |
| D. | 电解后溶液中c(H+)=4 mol/L |
8.如图甲、乙是两种重要的有机合成原料.下列有关说法中,不正确的是( )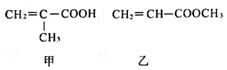
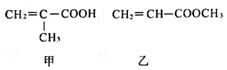
| A. | 甲与乙互为同分异构体 | |
| B. | 甲与乙都能与溴的四氯化碳溶液发生加成反应 | |
| C. | 甲与乙都能与金属钠反应产生氢气 | |
| D. | 在一定条件下,甲与乙均能发生取代反应 |
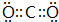 ,B与D形成的原子个数比为1:1的化合物的电子式是
,B与D形成的原子个数比为1:1的化合物的电子式是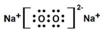 .
.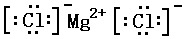 ; ②NaOH
; ②NaOH ;
;