题目内容
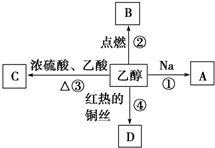 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物.写出下列反应的化学方程式及对应的反应类型:
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物.写出下列反应的化学方程式及对应的反应类型:反应①:
反应类型:
反应②:
反应类型:
反应③:
反应④:
考点:有机化学反应的综合应用
专题:有机反应
分析:由图可知,乙醇与钠反应生成乙醇钠,则A为乙醇钠,B为乙醇燃烧产物,应为二氧化碳和水,乙醇和乙酸在浓硫酸作用下反应生成乙酸乙酯,则C为乙酸乙酯,乙醇催化氧化生成乙醛,则D为乙醛,以此解答该题.
解答:
解:由图可知,乙醇与钠反应生成乙醇钠,则A为乙醇钠,B为乙醇燃烧产物,应为二氧化碳和水,乙醇易乙酸在浓硫酸作用下反应生成乙酸乙酯,则C为乙酸乙酯,乙醇催化氧化生成乙醛,则D为乙醛,
(1)反应①中,乙醇能和金属钠反应置换氢气,即2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,为置换反应;
反应②中,乙醇具有可燃性,燃烧方程式为:C2H6O+3O2
2CO2+3H2O,为氧化反应;
反应③为CH3COOH+C2H5OH
CH3COOC2H5+H2O,为 酯化(或取代)反应
反应④中乙醇能发生催化氧化反应,即2CH3CH2OH+O2
2CH3CHO+2H2O,为氧化反应;
故答案为:①2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑,置换反应;
②C2H6O+3O2
2CO2+3H2O,氧化反应;
③CH3COOH+C2H5OH
CH3COOC2H5+H2O,酯化(或取代)反应;
④2CH3CH2OH+O2
2CH3CHO+2H2O,氧化反应.
(1)反应①中,乙醇能和金属钠反应置换氢气,即2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,为置换反应;
反应②中,乙醇具有可燃性,燃烧方程式为:C2H6O+3O2
| 点燃 |
反应③为CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
反应④中乙醇能发生催化氧化反应,即2CH3CH2OH+O2
| 催化剂 |
| △ |
故答案为:①2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑,置换反应;
②C2H6O+3O2
| 点燃 |
③CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
④2CH3CH2OH+O2
| 催化剂 |
| △ |
点评:本题考查有机物推断,涉及烯烃、醇、醛、羧酸、酯的性质与转化,难度不大,有利于基础知识的巩固.

练习册系列答案
相关题目
下列实验基本操作正确的是( )
| A、用碱式滴定管量取0.10 mol?L-1的Na2CO3溶液22.10 mL |
| B、配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
| C、用广范pH试纸测某HCl溶液pH=3.6 |
| D、用玻璃棒蘸取HCl溶液滴到湿润的pH试纸上,测其pH |
用下列实验装置进行相应实验,能达到实验目的是( )
A、 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 制取少量乙烯气体 |
C、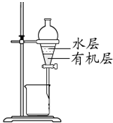 分离CCl4萃取溴水后已分层的有机层和水层 |
D、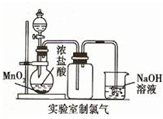 装置制取少量Cl2气体 |
下列实验操作不正确的是( )
| A、进行分液操作时,应将分液漏斗颈上的玻璃塞打开,或使塞上的凹槽(或小孔)对准漏斗上的小孔,打开旋塞,使下层液体慢慢沿烧杯壁流下,待下层液体完全流出后,关闭旋塞,上层液体从漏斗上口倒出 |
| B、蒸发操作中,边加热边用玻璃棒搅拌,当加热至蒸发皿中有较多固体析出时,应停止加热,利用余热将液体蒸干 |
| C、过滤操作中,滤纸边缘一定低于漏斗边缘,将玻璃棒靠在三层滤纸的边缘,将烧杯嘴靠在玻璃棒上,慢慢引流倒入液体 |
| D、在配制一定物质的量浓度的溶液的过程中,定容操作就是将蒸馏水注入容量瓶,当液面离容量瓶颈刻度线下2~3cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切 |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是( )
| A、AgNO3 (Ag2O) |
| B、NaOH(NaOH) |
| C、NaCl (盐酸) |
| D、CuSO4(Cu(OH)2) |