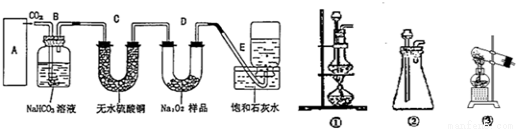
题目内容
下列说法错误的是
A.化学键的断裂和形成是化学反应中能量变化的主要原因
B.放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小
C.已知:S(s)+O2(g) = SO2(g) △H1 ;S(g)+O2(g) = SO2(g) △H2 ;则△H1>△H2
D.凡经加热而发生的化学反应都是吸热反应
D
【解析】
试题分析:A、化学反应的实质就是化学键的断裂与形成,化学反应都有能量变化,主要原因就是化学键的断裂与形成,正确;B、放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小,反应物总能量大的是放热反应,生成物总能量大的是吸热反应,正确;C、固体变为气体吸收热量,所以前者放出的热量少于后者,则△H1>△H2,正确;D、化学反应的热效应与反应条件无关,所以加热的反应不一定是吸热反应,错误,答案选D。
考点:考查化学反应与能量的关系

(12分)甲醇是重要的化学工业基础原料和液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度(℃) | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) | K3 | ||
(1)反应②是 (填“吸热”或“放热”)反应。
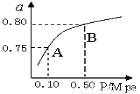
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。
(3)判断反应③△H 0; △S 0(填“>”“=”或“<”)据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。在500℃、2L的密闭容器中,进行反应③,测得某时刻H2、CO2、 CH3OH、H2O的物质的量分别为6mol、2 mol、10 mol、10 mol,此时v(正) v(逆) (填“>”“=”或“<”)
(4)甲醇燃料电池通常采用铂电极,其工作原理如图所示,负极的电极反应为: 。

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将0.2 mol/L的醋酸与0.1 mol/LBa(OH)2溶液等体积混合,则混合溶液中离子浓度由大到小的顺序为 。
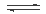
 CH3OH(g)
CH3OH(g)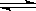 2C(g)在一密闭容器中进行,当改变下列条件之一时,一定能增大反应速率的是
2C(g)在一密闭容器中进行,当改变下列条件之一时,一定能增大反应速率的是
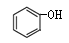 和
和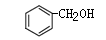 互为同系物
互为同系物