题目内容
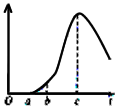
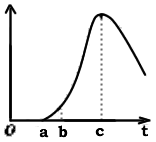
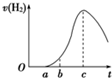 把空气中久置的铝片5.0g投入盛有500mL、0.5mol/L的硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用图所示的坐标曲线来表示.
把空气中久置的铝片5.0g投入盛有500mL、0.5mol/L的硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用图所示的坐标曲线来表示.(1)曲线0→a段不产生H2的原因
(2)曲线a→c段,产生氢气的速率增加较快的主要原因
(3)曲线c段以后,产生氢气的速率逐渐下降的主要原因
分析:(1)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,根据氧化铝的性质分析;
(2)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(3)溶液的浓度是影响化学反应速率的主要因素.
(2)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(3)溶液的浓度是影响化学反应速率的主要因素.
解答:解:(1)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,氧化铝首先稀硫酸反应生成氯化铝和水,不产生H2,离子方程式为Al2O3+6H+=2Al3++3H2O;
故答案为:金属铝表面的氧化铝与酸反应不产生氢气;有关化学方程式为 2Al+3H2SO4=Al2(SO4)3+3H2↑;
(2)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:该反应放热,温度对反应速率的影响大于浓度对反应速率的影响;
(3)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小,
故答案为:温度不变时浓度对反应速率的影响较大.
故答案为:金属铝表面的氧化铝与酸反应不产生氢气;有关化学方程式为 2Al+3H2SO4=Al2(SO4)3+3H2↑;
(2)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:该反应放热,温度对反应速率的影响大于浓度对反应速率的影响;
(3)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小,
故答案为:温度不变时浓度对反应速率的影响较大.
点评:本题考查了化学反应速率的影响因素,难度不大,注意根据图象分析理解随反应进行影响反应速率的主导元素.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
 把在空气中久置的铝片5.0g投入盛有500mL0,5mol?L-1盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL0,5mol?L-1盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题: