题目内容
可逆反应2NO2
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
| △ |
| A、NO2、NO和O2三者共存 |
| B、单位时间内生成n molO2的同时生成2n mol NO |
| C、容器中颜色不再变化 |
| D、容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析.
解答:
解:A、反应是可逆反应,反应混合物都为气体,过程中和平衡状态下三者共存,不能说明到达平衡状态,故A错误.
B、单位时间内生成n molO2的同时生成2n mol NO,是反应正向进行,不能说明反应达到平衡状态,故B错误;
C、NO2是红棕色,混合气体颜色不变,说明NO2浓度不变,确定反应达到平衡状态,故C正确;
D、反应达到平衡时的各物质的物质的量浓度与反应的初始物质的量浓度以及反应的转化程度有关,不能确定是否达到平衡,故D错误.
故选C.
B、单位时间内生成n molO2的同时生成2n mol NO,是反应正向进行,不能说明反应达到平衡状态,故B错误;
C、NO2是红棕色,混合气体颜色不变,说明NO2浓度不变,确定反应达到平衡状态,故C正确;
D、反应达到平衡时的各物质的物质的量浓度与反应的初始物质的量浓度以及反应的转化程度有关,不能确定是否达到平衡,故D错误.
故选C.
点评:本题考查化学平衡状态的判断,题目难度不大,做题时注意分析化学方程式的前后计量数大小的关系.

练习册系列答案
相关题目
下列对碱金属的叙述,其中完全不正确的组合是( )
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
| A、②③⑥ | B、②③④ |
| C、④⑤⑥ | D、①③⑤ |
密闭容器中的可逆反应 2HI(g)?I2(g)+H2(g),能说明反应达到平衡的是( )
| A、容器内压强不变 |
| B、单位时间内消耗2molHI,同时生成1molH2 |
| C、HI的浓度与I2的浓度相等 |
| D、混合气体的颜色不变 |
向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的PH( )
| A、大于7 | B、小于7 |
| C、恰好等于7 | D、上述情况都有可能 |
一定温度下,在体积可变的密闭容器中进行的可逆反应:C(s)+CO2(g)═2CO(g),不能判断反应已经达到化学平衡状态的是( )
| A、容器中总压强不变 |
| B、2v正(CO2)=v逆(CO) |
| C、C的质量不再变化 |
| D、容器中CO的体积分数不变 |
下列说法正确的是( )
| A、H2的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为142.9kJ?g-1,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ?mol-1 |
| B、反应A(g)═2B(g),若正反应的活化能为Ea kJ?mol-1,逆反应的活化能为Eb kJ?mol-1,则△H=(Ea-Eb)kJ?mol-1 |
| C、能自发进行的化学反应,一定是△H<0、△S>0 |
| D、增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
已知下列各组原子序数,其中能形成X2Y5型化合物的是( )
| A、17和13 | B、7和8 |
| C、15和17 | D、12和19 |
下列反应属于氧化还原反应的是( )
| A、二氧化碳和澄清石灰水反应 |
| B、铝和三氧化二铁高温下反应 |
| C、碳酸氢钠受热分解 |
| D、氧化铜和稀硫酸反应 |
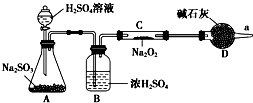 ①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).
①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).