题目内容
6.下列分子或离子的中心原子没有采取sp3杂化的是( )| A. | BF3 | B. | NH4+ | ||
| C. | CCl4 | D. | 晶体硅中的硅原子 |
分析 根据价层电子对互斥理论确定中心原子杂化类型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.中心原子的杂化类型为sp3,说明该分子中心原子的价层电子对个数是4,据此判断.
解答 解:A.BF3中B形成3个σ键,无孤电子对,B原子杂化轨道数=σ键数+孤对电子对数=3+0=3,所以采取sp2杂化,故A选;
B.NH4+中N原子杂化轨道数为$\frac{1}{2}$×(5+4-1)=4,采取sp3杂化方式,故B不选;
C.CCl4中C形成4个σ键,无孤电子对,为sp3杂化,故C不选;
D.晶体硅中的硅原子平均每个硅原子与四个邻近硅原子生成四个共价键,形成4个σ键,无孤电子对,硅原子杂化轨道数=σ键数+孤对电子对数=4+0=4,所以采取sp3杂化,故D不选;
故选A.
点评 本题考查了原子杂化方式的判断,根据价层电子对互斥理论来分析解答即可,明确价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb)中各个字母的含义是解本题的关键,题目难度中等.

练习册系列答案
相关题目
17.已知热化学方程式:
Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-351.5kJ•mol-1;
Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H=-90.84kJ•mol-1,
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H为( )
Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-351.5kJ•mol-1;
Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H=-90.84kJ•mol-1,
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H为( )
| A. | △H=+260.66 kJ•mol-1 | B. | △H=-260.66 kJ•mol-1 | ||
| C. | △H=-442.34 kJ•mol-1 | D. | △H=+442.34 kJ•mol-1 |
14.下列事实中,能说明苯环与侧链的相互影响会导致苯酚的化学性质与苯或醇不同的是( )
| A. | 1mol苯酚与3mol H2发生加成反应 | B. | 苯酚能和NaOH溶液反应 | ||
| C. | 苯酚燃烧产生带浓烟的火焰 | D. | 苯酚与浓溴水反应生成三溴苯酚 |
1.某学生做中和滴定实验的过程如下:
a.取一支碱式滴定管;
b.用蒸馏水洗净;
c.加入待测NaOH溶液;
d.记录液面刻度读数;
e.用酸式滴定管精确放出一定量标准酸液;
f.置于未经标准酸液润洗的洁净锥形瓶中;
g.加入适量蒸馏水;
h.加入酚酞试液2滴;
i.滴定时,边滴边摇动;
j.边注视滴定管内液面的变化;
k.当刚滴到溶液由无色变成粉红色时,即停止滴定;
l.记录液面读数;
m.根据滴定管的两次得出NaOH溶液的体积为22mL.
上述实验过程中的错误之处有( )
a.取一支碱式滴定管;
b.用蒸馏水洗净;
c.加入待测NaOH溶液;
d.记录液面刻度读数;
e.用酸式滴定管精确放出一定量标准酸液;
f.置于未经标准酸液润洗的洁净锥形瓶中;
g.加入适量蒸馏水;
h.加入酚酞试液2滴;
i.滴定时,边滴边摇动;
j.边注视滴定管内液面的变化;
k.当刚滴到溶液由无色变成粉红色时,即停止滴定;
l.记录液面读数;
m.根据滴定管的两次得出NaOH溶液的体积为22mL.
上述实验过程中的错误之处有( )
| A. | f.g.k.m | B. | c.j.k.m | C. | c.h.i.k | D. | f.g.h.j. |
11.下列物质中,不能发生水解反应的是( )
| A. | 油脂 | B. | 淀粉 | C. | 蔗糖 | D. | 葡萄糖 |
15.能用H++OH-═H2O表示的是( )
| A. | NaOH溶液和CO2的反应 | B. | Ba(OH)2溶液和稀硫酸的反应 | ||
| C. | NaOH溶液和稀硫酸反应 | D. | 氨水和稀硫酸的反应 |
16.在下列有机物中,能跟溴水发生加成反应,又能被酸性高锰酸钾溶液氧化的是( )
| A. | 乙烯 | B. | 苯 | C. | 甲苯 | D. | 乙烷 |
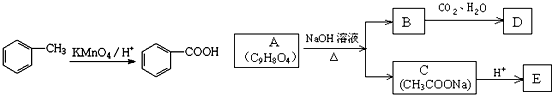
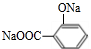 ,
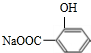
,

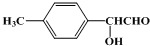 、
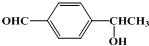
、
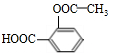 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$